题目内容
下列固体投入盐酸中,没有气体产生的是( )
| A、Na |
| B、Na2O |
| C、Na2O2 |
| D、Na2CO3 |
考点:钠的重要化合物
专题:几种重要的金属及其化合物
分析:A、钠和盐酸的反应方程式为:2Na+2HCl═2NaCl+H2↑;
B、氧化钠和盐酸的反应方程式为:Na2O+2HCl═2NaCl+H2O;
C、将Na2O2加入到盐酸溶液中,反应方程式为:2Na2O2+4HCl═4NaCl+2H2O+O2↑;
D、将Na2CO3加入到盐酸溶液中,反应方程式为:Na2CO3+2HCl═2NaCl+2H2O+CO2↑;
B、氧化钠和盐酸的反应方程式为:Na2O+2HCl═2NaCl+H2O;
C、将Na2O2加入到盐酸溶液中,反应方程式为:2Na2O2+4HCl═4NaCl+2H2O+O2↑;
D、将Na2CO3加入到盐酸溶液中,反应方程式为:Na2CO3+2HCl═2NaCl+2H2O+CO2↑;
解答:
解:A、钠和盐酸的反应方程式为:2Na+2HCl═2NaCl+H2↑,所以有氢气生成,故A错误;
B、氧化钠和盐酸的反应方程式为:Na2O+2HCl═2NaCl+H2O,没有气体生成,故B正确;
C、将Na2O2加入到盐酸溶液中,反应方程式为:2Na2O2+4HCl═4NaCl+2H2O+O2↑,有氧气生成,故C错误;
D、将Na2CO3加入到盐酸溶液中,反应方程式为:Na2CO3+2HCl═2NaCl+2H2O+CO2↑,有二氧化碳气体生成,故D错误;
故选:B.
B、氧化钠和盐酸的反应方程式为:Na2O+2HCl═2NaCl+H2O,没有气体生成,故B正确;
C、将Na2O2加入到盐酸溶液中,反应方程式为:2Na2O2+4HCl═4NaCl+2H2O+O2↑,有氧气生成,故C错误;
D、将Na2CO3加入到盐酸溶液中,反应方程式为:Na2CO3+2HCl═2NaCl+2H2O+CO2↑,有二氧化碳气体生成,故D错误;
故选:B.
点评:本题考查了钠及化合物的性质,难度不大,注意根据方程式分析反应即可.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、将淀粉与稀硫酸加热一段时间后,欲检验淀粉已经水解,可直接加入银氨溶液 |
B、有机物  的消去产物有两种 的消去产物有两种 |
| C、某有机化合物相对分子质量为109,将该化合物在强碱水溶液中水解后先用HNO3酸化,再用AgNO3溶液,结果生成淡黄色沉淀,则该有机物可能为C3H7Br |
| D、可用溴水鉴别甲苯、苯酚、1-己烯、淀粉碘化钾溶液、四氯化碳等 |
下列分子中,所有原子都可能处在同一平面的是( )
| A、1,3-丁二烯 | B、丙炔 |
| C、环已烯 | D、甲苯 |
有等体积、等pH的Ca(OH)2、KOH和NH3?H2O三种碱溶液,滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为V1、V2、V3,则三者的大小关系正确的是( )
| A、V3>V2=V1 |
| B、V3=V2=V1 |
| C、V3>V2>V1 |
| D、V1=V2>V3 |
下列叙述正确的是( )
| A、二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
| B、某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I- |
| C、向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体 |
| D、将SO2通入品红溶液,溶液褪色后加热恢复原色,将SO2通入溴水,溴水褪色后加热也能恢复原色 |
根据元素周期表和元素周期律分析下面的推断,其中正确的是( )
| A、锂、钠、钾的原子半径逐渐增大 |
| B、钠比镁活泼 |
| C、溴单质的氧化性比氯气强 |
| D、氢氧化钠比氢氧化钾的碱性强 |
下列反应中生成物总能量高于反应物总能量的是( )
| A、碳酸钙受热分解 |
| B、乙醇燃烧 |
| C、铝粉与盐酸反应 |
| D、中和反应 |
 某物质只含C、H、O三种元素,其分子模型如右图所示,分子中共有12个原子(图中球与球之间的连线代表化学键:单键、双键等).
某物质只含C、H、O三种元素,其分子模型如右图所示,分子中共有12个原子(图中球与球之间的连线代表化学键:单键、双键等).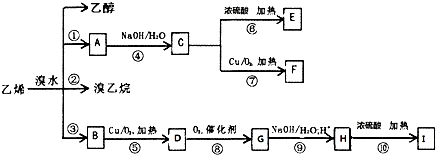
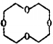 I的分子式为C4H4O4,是一种环状化合物.请回答下列问题:
I的分子式为C4H4O4,是一种环状化合物.请回答下列问题: