题目内容
下列溶液中H+浓度为0.01mol/L的是( )
| A、0.01mol/L的CH3COOH |
| B、0.01mol/LHCl0 |
| C、0.01mol/LHF |
| D、0.005mol/LH2SO4 |
考点:弱电解质在水溶液中的电离平衡,物质的量浓度的相关计算
专题:
分析:A、CH3COOH是弱电解质,部分电离;
B、HCl0是弱电解质,部分电离;
C、HF是弱电解质,部分电离;
D、硫酸是二元强酸,完全电离.
B、HCl0是弱电解质,部分电离;
C、HF是弱电解质,部分电离;
D、硫酸是二元强酸,完全电离.
解答:
A、CH3COOH是弱电解质,部分电离,所以0.01mol/L的CH3COOH,所以H+浓度小于0.01mol/L,故A错误;
B、HCl0是弱电解质,部分电离,所以0.01mol/L的HCl0,所以H+浓度小于0.01mol/L,故B错误;
C、HF是弱电解质,部分电离,所以0.01mol/L的HF,所以H+浓度小于0.01mol/L,故C错误;
D、硫酸是二元强酸,完全电离,所以0.005mol/LH2SO4,所以H+浓度为0.01mol/L,故D正确;
故选D.
B、HCl0是弱电解质,部分电离,所以0.01mol/L的HCl0,所以H+浓度小于0.01mol/L,故B错误;
C、HF是弱电解质,部分电离,所以0.01mol/L的HF,所以H+浓度小于0.01mol/L,故C错误;
D、硫酸是二元强酸,完全电离,所以0.005mol/LH2SO4,所以H+浓度为0.01mol/L,故D正确;
故选D.
点评:本题考查电解质的强弱,强电解质完全电离,弱电解质部分电离,要注意硫酸是二元强酸,比较容易.

练习册系列答案
相关题目
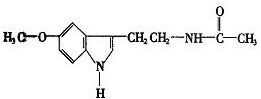 脑白金的主要作用是改善睡眠和润肠通便,主要成分是褪黑素(Melatonin)和低聚糖,其有效成分的结构简式如图,下列对该化合物的叙述正确的是( )
脑白金的主要作用是改善睡眠和润肠通便,主要成分是褪黑素(Melatonin)和低聚糖,其有效成分的结构简式如图,下列对该化合物的叙述正确的是( )①它属于芳香烃
②分子式为C15N2H16O2
③可以使酸性高锰酸钾溶液褪色
④不可以发生水解反应.
| A、②③ | B、③ | C、③④ | D、①②④ |
常温下,将pH=3的盐酸与pH=9的Ba(OH)2溶液混合,若要得到pH=7的溶液,混合时盐酸与Ba(OH)2溶液的体积比为( )
| A、1:60 | B、3:1 |
| C、100:1 | D、1:100 |
欲除去氢氧化钠溶液中混有的少量碳酸钠,下列方法中最适当的是( )
| A、加入适量的稀硫酸 |
| B、加入适量的盐酸 |
| C、加入适量的氢氧化钙溶液 |
| D、加入适量的氯化钙溶液 |
晶体与非晶体的本质区别在于( )
| A、是否有规则的几何外形 |
| B、是否有各向异性 |
| C、是否有固定的熔点 |
| D、微粒是否呈周期性的有序排列 |
下列反应的离子方程式书写正确的是 ( )
| A、氟气通入水中:2F2+2H2O═4F-+4H++O2 |
| B、向小苏打溶液中加入过量的石灰水:Ca2++2OH-+2HCO3-═CaCO3↓+CO32-+2H2O |
| C、硫氢化钠溶液与盐酸反应:S2-+2H+═H2S↑? |
| D、FeBr2溶液与等摩Cl2反应:2Fe2++2Br-+2Cl2═2Fe3++4Cl-+Br2 |