题目内容
 一定条件下将2.3mol SO2气体和1.2mol O2气体充入一容积可变的密闭容器中,可滑动活塞的位置如图1所示,在恒温恒压下发生如下反应:2SO2(g)+O2(g)?2SO3(g),其中△H<0,当反应达到平衡时,活塞位置如图2所示.
一定条件下将2.3mol SO2气体和1.2mol O2气体充入一容积可变的密闭容器中,可滑动活塞的位置如图1所示,在恒温恒压下发生如下反应:2SO2(g)+O2(g)?2SO3(g),其中△H<0,当反应达到平衡时,活塞位置如图2所示.(1)平衡时SO2转化率为
(2)该条件下反应的平衡常数为
(3)讨论温度对该反应中SO2转化率的影响
考点:化学平衡的计算
专题:化学平衡专题
分析:(1)恒压容器中开始到平衡体积比等于物质的量之比,依据化学方程式计算得到,转化率=
×100%;
(2)依据平衡三段式计算平衡浓度,结合平衡常数概念列式计算得到反应的平衡常数;
(3)反应是放热反应,温度升高,平衡逆向进行,二氧化硫转化率减小.
| 消耗量 |
| 起始量 |
(2)依据平衡三段式计算平衡浓度,结合平衡常数概念列式计算得到反应的平衡常数;
(3)反应是放热反应,温度升高,平衡逆向进行,二氧化硫转化率减小.
解答:
解:一定条件下将2.3mol SO2气体和1.2mol O2气体充入一容积可变的密闭容器中,可滑动活塞的位置如图1所示,在恒温恒压下发生如下反应:2SO2(g)+O2(g)?2SO3(g),其中△H<0,当反应达到平衡时,活塞位置如图2所示,气体体积减小7L-5L=2L,
由体积比等于物质的量之比得到(2.3mol+1.2mol):n=7:5,
解得n=2.5mol,
反应前后减少3.5mol-2.5mol=1mol,反应的二氧化硫为2mol,
二氧化硫转化率=
×100%=87%,
故答案为:87%;
(2)平衡后气体体积为5L,则
2SO2(g)+O2(g)?2SO3(g),
起始量(mol) 2.3 1.2 0
变化量(mol) 2 1 2
平衡量(mol) 0.3 0.2 2
平衡常数K=
=0.00111=1.11×103;
故答案为:1.11×103;
(3)反应是放热反应,温度升高,平衡逆向进行,二氧化硫转化率减小,故答案为:升高温度,SO2转化率降低.
由体积比等于物质的量之比得到(2.3mol+1.2mol):n=7:5,
解得n=2.5mol,
反应前后减少3.5mol-2.5mol=1mol,反应的二氧化硫为2mol,
二氧化硫转化率=
| 2mol |
| 2.3mol |
故答案为:87%;
(2)平衡后气体体积为5L,则
2SO2(g)+O2(g)?2SO3(g),
起始量(mol) 2.3 1.2 0
变化量(mol) 2 1 2
平衡量(mol) 0.3 0.2 2
平衡常数K=
(
| ||||
(
|
故答案为:1.11×103;
(3)反应是放热反应,温度升高,平衡逆向进行,二氧化硫转化率减小,故答案为:升高温度,SO2转化率降低.
点评:本题考查了化学平衡分析,影响因素的分析应用和计算,平衡常数计算和转化率的计算式解题关键,注意恒压容器中的特征,题目难度中等.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
分子中碳原子数相等的下列各类物质,各取1mol,在充足的氧气中完全燃烧,耗氧量最大的是( )
| A、苯的同系物 | B、烷烃 |
| C、烯烃 | D、炔烃 |
下列各组离子可以大量共存的是( )
| A、Na+、Ba2+、SO42-、Cl- |
| B、H+、Ag+、Cl-、NO3- |
| C、K+、H+、CO32-、Cl- |
| D、Cu2+、Fe3+、Cl-、NO3- |
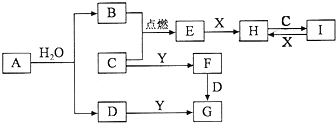 有关物质的转化关系如图所示(部分物质和条件已略去).B、C、E是常见气体;A、X、Y是常见金属单质,其中Y既能与强酸反应,又能与强碱反应;G的焰色反应显黄色;I的溶液呈黄色.
有关物质的转化关系如图所示(部分物质和条件已略去).B、C、E是常见气体;A、X、Y是常见金属单质,其中Y既能与强酸反应,又能与强碱反应;G的焰色反应显黄色;I的溶液呈黄色.
 在两份体积相同的NaOH溶液A、B中,分别通入CO2气体,充分反应后,在所得溶液中分别加入1mol/L的盐酸,所加盐酸体积(mL)与产生CO2气体的体积(L)的关系如图所示.试填写下列空白:
在两份体积相同的NaOH溶液A、B中,分别通入CO2气体,充分反应后,在所得溶液中分别加入1mol/L的盐酸,所加盐酸体积(mL)与产生CO2气体的体积(L)的关系如图所示.试填写下列空白: b.
b. c.
c.
 b.
b. c.
c.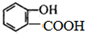
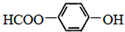
 的名称为
的名称为 核磁共振氢谱有
核磁共振氢谱有 .
. 一化学研究性学习小组对某工厂生产印刷电路板后所得废液进行探究(生产原理:2Fe3++Cu═2Fe2++Cu2+).请按要求完成下列探究报告.
一化学研究性学习小组对某工厂生产印刷电路板后所得废液进行探究(生产原理:2Fe3++Cu═2Fe2++Cu2+).请按要求完成下列探究报告.