题目内容
PM2.5是指大气中直径d≤2.5μm的可入肺颗粒,含水溶性离子、痕量重金属、粉尘等.
(1)水溶性离子主要由铵盐、硝酸盐、硫酸盐等组成.
①氮原子的结构示意图为
②硫酸盐是硫和短周期元素A、B形成的A2S和SB2等化合物经过一系列化学反应生成的,A元素周期数是族序数的3倍,B元素原子的最外层电子数是次外层的3倍,SB2的化学式为 ,AHS的水溶液显碱性的原因用离子方程式表示为 .
③火箭推进器使用联氨(N2H4)和过氧化氢作为推进剂可以减少污染,已知:
N2H4(l)+2H2O2(l)=N2(g)+4H2O(l)△H=-993.6kJ?mol-1
2H2O2(l)=2H2O(l)+O2(g)△H=-196.4kJ?mol-1
则常温下N2H4在氧气中燃烧生成无污染物质的热化学方程式为 .
(2)痕量重金属主要包含Fe、Zn等元素,大多来自生产生活.
①K2FeO4是生活中的新型净水剂,可用NaClO、Fe(OH)3和KOH制取,其反应的化学方程式为 .
②用K2FeO4和Zn可制高能可充电电池,其总反应式为:3Zn+2k2FeO4+8H2O?3Zn(OH)2+2Fe(OH)3+4KOH
则充电时阴极的电极反应式为 .
(1)水溶性离子主要由铵盐、硝酸盐、硫酸盐等组成.
①氮原子的结构示意图为
②硫酸盐是硫和短周期元素A、B形成的A2S和SB2等化合物经过一系列化学反应生成的,A元素周期数是族序数的3倍,B元素原子的最外层电子数是次外层的3倍,SB2的化学式为
③火箭推进器使用联氨(N2H4)和过氧化氢作为推进剂可以减少污染,已知:
N2H4(l)+2H2O2(l)=N2(g)+4H2O(l)△H=-993.6kJ?mol-1
2H2O2(l)=2H2O(l)+O2(g)△H=-196.4kJ?mol-1
则常温下N2H4在氧气中燃烧生成无污染物质的热化学方程式为
(2)痕量重金属主要包含Fe、Zn等元素,大多来自生产生活.
①K2FeO4是生活中的新型净水剂,可用NaClO、Fe(OH)3和KOH制取,其反应的化学方程式为
②用K2FeO4和Zn可制高能可充电电池,其总反应式为:3Zn+2k2FeO4+8H2O?3Zn(OH)2+2Fe(OH)3+4KOH
则充电时阴极的电极反应式为
分析:(1)①根据原子结构示意图的表示方法;
②硫酸盐是硫和短周期元素A、B形成的A2S和SB2等化合物经过一系列化学反应生成的,A元素周期数是族序数的3倍,则A为钠,B元素原子的最外层电子数是次外层的3倍,则B为氧;溶液呈碱性说明酸式酸根离子电离的程度小于水解程度,水解导致氢氧根离子浓度大于氢离子浓度而使溶液呈碱性;
③根据已知热化学方程式和目标反应的热化学反应方程式,利用盖斯定律来解答;
(2)①根据根据化合价升降、质量守恒确定产物,然后根据电子得失守恒配平;
②根据充电时,阴极上氢氧化锌得电子发生还原反应.
②硫酸盐是硫和短周期元素A、B形成的A2S和SB2等化合物经过一系列化学反应生成的,A元素周期数是族序数的3倍,则A为钠,B元素原子的最外层电子数是次外层的3倍,则B为氧;溶液呈碱性说明酸式酸根离子电离的程度小于水解程度,水解导致氢氧根离子浓度大于氢离子浓度而使溶液呈碱性;
③根据已知热化学方程式和目标反应的热化学反应方程式,利用盖斯定律来解答;
(2)①根据根据化合价升降、质量守恒确定产物,然后根据电子得失守恒配平;
②根据充电时,阴极上氢氧化锌得电子发生还原反应.
解答:解:(1)①氮原子的结构示意图为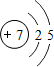 ,故答案为:
,故答案为: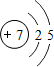 ;
;
②B元素原子的最外层电子数是次外层的3倍,则B为氧,所以SB2的化学式为SO2;
溶液呈碱性说明酸式酸根离子电离的程度小于水解程度,水解导致氢氧根离子浓度大于氢离子浓度而使溶液呈碱性,水解方程式为HS-+H2O?H2S+OH-,
故答案为:SO2;HS-+H2O?H2S+OH-;
③N2H4(l)+2H2O2(l)=N2(g)+4H2O(l)△H=-993.6kJ?mol-1 ①
2H2O2(l)=2H2O(l)+O2(g)△H=-196.4kJ?mol-1 ②
则常温下N2H4在氧气中燃烧生成无污染物质的热化学方程式可用①-②:N2H4(l)+O2(l)=N2(g)+2H2O(g)△H=-797.2kJ?mol-1,
故答案为:N2H4(l)+O2(l)=N2(g)+2H2O(g)△H=-797.2kJ?mol-1;
(2)①NaClO、Fe(OH)3和KOH反应得到高铁酸钾,氯化钠和水,反应的化学方程式为:2Fe(OH)3+3NaClO+4KOH=2K2FeO4+3NaCl+5H2O,
故答案为:2Fe(OH)3+3NaClO+4KOH=2K2FeO4+3NaCl+5H2O;
②充电时,阴极上氢氧化锌得电子发生还原反应:Zn(OH)2+2e-=Zn+2OH-,故答案为:Zn(OH)2+2e-=Zn+2OH-.
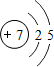 ,故答案为:
,故答案为: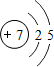 ;
;②B元素原子的最外层电子数是次外层的3倍,则B为氧,所以SB2的化学式为SO2;
溶液呈碱性说明酸式酸根离子电离的程度小于水解程度,水解导致氢氧根离子浓度大于氢离子浓度而使溶液呈碱性,水解方程式为HS-+H2O?H2S+OH-,
故答案为:SO2;HS-+H2O?H2S+OH-;
③N2H4(l)+2H2O2(l)=N2(g)+4H2O(l)△H=-993.6kJ?mol-1 ①
2H2O2(l)=2H2O(l)+O2(g)△H=-196.4kJ?mol-1 ②
则常温下N2H4在氧气中燃烧生成无污染物质的热化学方程式可用①-②:N2H4(l)+O2(l)=N2(g)+2H2O(g)△H=-797.2kJ?mol-1,
故答案为:N2H4(l)+O2(l)=N2(g)+2H2O(g)△H=-797.2kJ?mol-1;
(2)①NaClO、Fe(OH)3和KOH反应得到高铁酸钾,氯化钠和水,反应的化学方程式为:2Fe(OH)3+3NaClO+4KOH=2K2FeO4+3NaCl+5H2O,
故答案为:2Fe(OH)3+3NaClO+4KOH=2K2FeO4+3NaCl+5H2O;
②充电时,阴极上氢氧化锌得电子发生还原反应:Zn(OH)2+2e-=Zn+2OH-,故答案为:Zn(OH)2+2e-=Zn+2OH-.
点评:本题主要考查了盐类的水解、盖斯定律的运用、氧化还原等知识,难度不大,注意知识的掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2012年2月29日,新发布的《环境空气质量标准》中增加了PM2.5监测指标.PM2.5是指大气中直径小于或等于2.5μm的颗粒物,其主要来源之一是化石燃料的燃烧.下列措施不能减少PM2.5污染的是( )
| A、鼓励使用液化石油气做燃料 | B、鼓励使用太阳能、风能等清洁能源 | C、鼓励水力、核能发电,少用煤火力发电 | D、鼓励坐公交车出行,少用私家车 |