题目内容
1.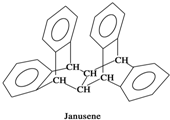 如图是一种形状酷似罗马两面神Janus的有机物结构简式,化学家建议将该分子叫做“Janusene”,下列说法正确的是( )
如图是一种形状酷似罗马两面神Janus的有机物结构简式,化学家建议将该分子叫做“Janusene”,下列说法正确的是( )| A. | Janusene的分子式为C30H20 | |
| B. | Janusene属于苯的同系物 | |
| C. | Janusene苯环上的一氯代物有8种 | |
| D. | Janusene既可发生氧化反应,又可发生还原反应 |
分析 A.根据结构数出C原子、H原子数目,据此写出分子式.注意根据C的四价结构确定H原子;
B.苯的同系物含有1个苯环、侧链为烷基;
C.根据等效H原子判断,有几种H原子,其一氯代物就有几种;
D.属于烃能燃烧,含有苯环可以与氢气发生加成反应.
解答 解:A.根据有机物结构可知分子中含有30个C原子、22个H原子,所以该有机物分子式为C30H22,故A错误;
B.苯的同系物含有1个苯环、侧链为烷基,该有机物含有4个苯环,故不是苯的同系物,故B错误;
C.图中竖直方向的两个苯环对称,其中每个苯环含有4个H原子,两两对称,即每个苯环含有2种H原子,同理,横向的两个苯环也含有2种H原子,故该有机物分子中苯环含有4种H原子,苯环上的一氯代物有4种,故C错误;
D、该有机物属于烃能燃烧,属于氧化反应,分子中含有苯环,可以与氢气发生加成反应,属于还原反应,故D正确;
故选:D.
点评 本题考查有机物的结构、同分异构体、苯的同系物等,难度中等,注意苯的同系物含有1个苯环、侧链为烷基,难点是其一氯代物同分异构体种类判断.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
将A和B加入密闭容器中,在一定条件下发生反应:A(g)+B(s) 2C(g),忽略固体体积,平衡时C的体积分数
2C(g),忽略固体体积,平衡时C的体积分数 (%)随温度和压强的变化如下表所示:
(%)随温度和压强的变化如下表所示:
压强/MPa 体积分数/% 温度/℃ | 1.0 | 2.0 | 3.0 |
800 | 54.0 | a | b |
900 | c | 75.0 | d |
1000 | e | f | 83.0 |
①a﹤b ②该反应的熵变△S﹤0 ③900℃、2.0MPa时A的转化率为60%
④K(1000℃)﹥K(800℃) ⑤正反应为吸热反应 上述①~⑤中正确的有( )
A.4个 B.3个 C.2个 D.1个
6.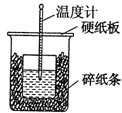 50mL 0.55mol•L-1盐酸与50mL 0.50mol•L-1NaOH溶液在如图的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
50mL 0.55mol•L-1盐酸与50mL 0.50mol•L-1NaOH溶液在如图的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是环形玻璃搅拌棒.
(2)从装置图上看除了缺少一种玻璃仪器外,还有一处不妥的是:碎纸条未填满,大小烧杯杯口未相平.
(3)若实验中改用50mL 0.55mol•L-1醋酸溶液进行反应,与上述实验相比,所放出的热量减小(填“减少”“不变”“增多”);
(4)若实验改用25mL 0.55mol•L-1硫酸与25mL 0.50mol•L-1Ba(OH)2溶液代替上述反应,所求得的中和热△H偏小 (填“偏大”“偏小”“无影响”).
(5)已知:Q=cm△t,如果盐酸和NaOH溶液的密度均为1g•cm-3,反应后混合溶液的比热容c=4.18J•(g•℃)-1.实验数据如表:根据上表中所测数据,通过计算得到中和热△H=-56.8kJ/mol(保留一位小数).
(6)下列操作能引起△H偏大的是:①②③(填序号)操作.
①大烧杯上不盖硬纸板
②用环形铜丝搅拌棒搅拌反应混合溶液
③分多次把NaOH溶液倒入装盐酸的小烧杯中.
 50mL 0.55mol•L-1盐酸与50mL 0.50mol•L-1NaOH溶液在如图的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
50mL 0.55mol•L-1盐酸与50mL 0.50mol•L-1NaOH溶液在如图的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:(1)从实验装置上看,图中尚缺少的一种玻璃仪器是环形玻璃搅拌棒.
(2)从装置图上看除了缺少一种玻璃仪器外,还有一处不妥的是:碎纸条未填满,大小烧杯杯口未相平.
(3)若实验中改用50mL 0.55mol•L-1醋酸溶液进行反应,与上述实验相比,所放出的热量减小(填“减少”“不变”“增多”);
(4)若实验改用25mL 0.55mol•L-1硫酸与25mL 0.50mol•L-1Ba(OH)2溶液代替上述反应,所求得的中和热△H偏小 (填“偏大”“偏小”“无影响”).
(5)已知:Q=cm△t,如果盐酸和NaOH溶液的密度均为1g•cm-3,反应后混合溶液的比热容c=4.18J•(g•℃)-1.实验数据如表:根据上表中所测数据,通过计算得到中和热△H=-56.8kJ/mol(保留一位小数).
| 实验 次数 | 起始温度t1/℃ | 终止温度t2/℃] | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.3 | 20.3 | 23.6 |
| 2 | 20.3 | 20.3 | 23.7 |
| 3 | 20.3 | 20.3 | 25.9 |
| 4 | 20.3 | 20.3 | 23.8 |
①大烧杯上不盖硬纸板
②用环形铜丝搅拌棒搅拌反应混合溶液
③分多次把NaOH溶液倒入装盐酸的小烧杯中.
13.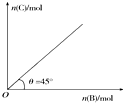 盛有足量A的体积固定的密闭容器中加入B,发生反应:A(s)+2B(g)?4C(g)+D(g)△H<0.一定条件下达到平衡时,C的物质的量与加入的B的物质的量的变化关系如图所示.下列说法不正确的是( )
盛有足量A的体积固定的密闭容器中加入B,发生反应:A(s)+2B(g)?4C(g)+D(g)△H<0.一定条件下达到平衡时,C的物质的量与加入的B的物质的量的变化关系如图所示.下列说法不正确的是( )
 盛有足量A的体积固定的密闭容器中加入B,发生反应:A(s)+2B(g)?4C(g)+D(g)△H<0.一定条件下达到平衡时,C的物质的量与加入的B的物质的量的变化关系如图所示.下列说法不正确的是( )
盛有足量A的体积固定的密闭容器中加入B,发生反应:A(s)+2B(g)?4C(g)+D(g)△H<0.一定条件下达到平衡时,C的物质的量与加入的B的物质的量的变化关系如图所示.下列说法不正确的是( )| A. | 降低温度,则图中θ>45° | |
| B. | 平衡后再加入B,正反应速率增大,逆反应速率减小 | |
| C. | 平衡时B的转化率为50% | |
| D. | 平衡后再加入A,体系内气体密度不变 |
10.氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为:a HClO3→b O2↑+c Cl2↑+d HClO4+e H2O,用湿润的淀粉碘化钾试纸检验气体产物时,试纸先变蓝后褪色.下列说法错误的是( )
| A. | 由反应可确定:氧化性HClO3>HClO4 | |
| B. | 变蓝的淀粉碘化钾试纸褪色是因为可能发生了:4C12+I2+6H2O→12H++8Cl-+2IO3- | |
| C. | 若氯酸分解所得的混合气体的平均摩尔质量为47.6g/mol,则反应方程式可表示为:26HClO3→15O2↑+8C12↑+10HClO4+8H2O | |
| D. | 若化学计量数a=8,b=3,则该反应转移电子数为20e |
11.下列离子方程式正确的是( )
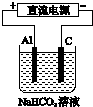
| A. | 用Al作电极电解NaHCO3溶液:2Al+6H2O═2Al(OH)3↓+3H2↑ | |
| B. | 向明矾溶液中加入氢氧化钡溶液至沉淀质量最大时:2Al3++2SO42-+2Ba2++6OH-═2BaSO4↓+2Al(OH)3↓ | |
| C. | 碳酸钠的水解反应:CO32-+H3O+═HCO3-+H2O | |
| D. | 酸性高锰酸钾溶液与双氧水反应:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O |
 某蓄电池的反应为NiO2+Fe+2H2O$?_{放电}^{充电}$Fe(OH)2+Ni(OH)2.
某蓄电池的反应为NiO2+Fe+2H2O$?_{放电}^{充电}$Fe(OH)2+Ni(OH)2.