题目内容
某溶液能溶解Al(OH)3,不能溶解SiO2,在该溶液中可以大量共存的离子组是( )
| A、I-、Na+、Cl-、NO3- |
| B、Fe3+、Ca2+、CH3COO-、HCO3- |
| C、Na+、Mg2+、NO3-、SO42- |
| D、Ba2+、K+、Cl-、SO42- |
考点:离子共存问题
专题:离子反应专题
分析:能溶解Al(OH)3,该溶液为酸性或者强碱性溶液,不能溶解SiO2,则该溶液一定为酸性溶液,
A.酸性条件下硝酸根离子具有强氧化性,能够氧化碘离子;
B.铁离子与碳酸氢根离子发生双水解反应,醋酸根离子、碳酸氢根离子与氢离子反应;
C.Na+、Mg2+、NO3-、SO42-离子之间不发生反应,也不与酸性溶液中的氢离子反应;
D.钡离子与硫酸根离子反应生成硫酸钡沉淀.
A.酸性条件下硝酸根离子具有强氧化性,能够氧化碘离子;
B.铁离子与碳酸氢根离子发生双水解反应,醋酸根离子、碳酸氢根离子与氢离子反应;
C.Na+、Mg2+、NO3-、SO42-离子之间不发生反应,也不与酸性溶液中的氢离子反应;
D.钡离子与硫酸根离子反应生成硫酸钡沉淀.
解答:
解:能溶解Al(OH)3,该溶液为酸性或者强碱性溶液,不能溶解SiO2,则该溶液一定为酸性溶液,溶液中存在大量氢离子,
A.NO3-在酸性溶液中能够氧化I-,在溶液中不能大量共存,故A错误;
B.Fe3+、HCO3-之间发生双水解反应,CH3COO-、HCO3-与氢离子反应,在溶液中不能大量共存,故B错误;
C.Na+、Mg2+、NO3-、SO42-离子之间不反应,且都不与氢离子反应,在溶液中能够大量共存,故C正确;
D.Ba2+、SO42-之间反应生成难溶物硫酸钡,在溶液中不能大量共存,故D错误;
故选C.
A.NO3-在酸性溶液中能够氧化I-,在溶液中不能大量共存,故A错误;
B.Fe3+、HCO3-之间发生双水解反应,CH3COO-、HCO3-与氢离子反应,在溶液中不能大量共存,故B错误;
C.Na+、Mg2+、NO3-、SO42-离子之间不反应,且都不与氢离子反应,在溶液中能够大量共存,故C正确;
D.Ba2+、SO42-之间反应生成难溶物硫酸钡,在溶液中不能大量共存,故D错误;
故选C.
点评:本题考查离子共存判断,题目难度中等,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间等;解决离子共存问题时还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,正确理解“能溶解Al(OH)3,不能溶解SiO2”的含义为解答关键.

练习册系列答案
相关题目
用足量的CO还原32.0g某铁氧化物,将生成的气体通入足量澄清石灰水中,得到60g沉淀,则该氧化物是( )
| A、FeO |
| B、Fe2O3 |
| C、Fe3O4 |
| D、无法计算 |
下列各组离子,在强酸性溶液中可以大量共存的是( )
| A、Na+、Ba2+、SO42- |
| B、Ag+、K+、NO3- |
| C、Ba2+、HCO3-、NO3- |
| D、Na+、NO3-、CO32- |
在新制的氯水中存在平衡:Cl2+H2O?H++Cl-+HClO,若向氯水中投入少量碳酸钙粉末,溶液中发生的变化是( )
| A、H+浓度减小,HClO浓度减小 |
| B、H+浓度增大,HClO浓度增大 |
| C、H+浓度增大,HClO浓度减小 |
| D、H+浓度减小,HClO浓度增大 |
0.3mol Cu2S与足量的浓硝酸反应,生成硝酸铜、硫酸、二氧化氮和水.则参加反应的硝酸中,被还原的硝酸的物质的量为( )
| A、0.6mol |
| B、1.2mol |
| C、2.2mol |
| D、3.0mol |
某温度下已知反应mX(g)+nY(g)?qZ(g)△H=+Q kJ?mol-1(Q>0),下列叙述正确的是( )
A、反应速率υ正(X)=
| ||
| B、降低温度,反应的速率值变大 | ||
| C、反应达到最大限度时,加入X,反应的△H增大 | ||
| D、在一定条件下向容器中放入m molX和n mol Y,充分反应吸收Q kJ的能量 |
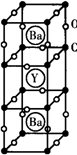 1986年,瑞士两位科学家发现一种性能良好的金属氧化物超导体,使超导工作取得突破性进展,为此两位科学家获得了1987年的Nobel物理学奖.其晶胞结构如图.
1986年,瑞士两位科学家发现一种性能良好的金属氧化物超导体,使超导工作取得突破性进展,为此两位科学家获得了1987年的Nobel物理学奖.其晶胞结构如图.