题目内容
如表是元素周期表的一部分,针对表中的①~⑧种元素,填写下列空白.
(1)在这些元素中,化学性质最不活泼的是 (填元素符号)这种元素的原子结构示意图为 ;
(2)用电子式表示元素⑦的单质分子的形成过程 ;
(3)在非金属元素的最高价氧化物所对应的水化物中,酸性最强的化合物是 (填化学式).在金属元素氧化物所对应的水化物中,碱性最强的化合物是 (填化学式),具有两性的化合物是 (填化学式);
(4)元素③的氢化物的电子式为 .元素③的氢化物分别跟元素④、元素⑦的单质反应的化学方程式是 、 .
| 主族 周期 |
IA | IIA | IIIA | IVA | VA | VIA | VIIA | O |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(2)用电子式表示元素⑦的单质分子的形成过程
(3)在非金属元素的最高价氧化物所对应的水化物中,酸性最强的化合物是
(4)元素③的氢化物的电子式为
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:根据元素在周期表中的位置知,①②③④⑤⑥⑦⑧分别是C、N、O、Na、Al、S、Cl、Ar元素,
(1)稀有气体元素的化学性质最不活泼,所以Ar是最不活泼的元素,Ar原子核外有3个电子层、最外层电子数是8,据此写出其原子结构示意图;
(2)氯原子之间通过共用电子对形成氯气分子;
(3)元素的非金属性越强,其最高价氧化物的水化物酸性越强;金属性越强的元素,其对应的最高价氧化物的水化物碱性越强;氢氧化铝具有两性;
(4)元素③的氢化物是水,水分子中每个氢原子和氧原子之间形成共价键;钠和水反应生成NaOH、氯气和水反应生成HCl和HClO.
(1)稀有气体元素的化学性质最不活泼,所以Ar是最不活泼的元素,Ar原子核外有3个电子层、最外层电子数是8,据此写出其原子结构示意图;
(2)氯原子之间通过共用电子对形成氯气分子;
(3)元素的非金属性越强,其最高价氧化物的水化物酸性越强;金属性越强的元素,其对应的最高价氧化物的水化物碱性越强;氢氧化铝具有两性;
(4)元素③的氢化物是水,水分子中每个氢原子和氧原子之间形成共价键;钠和水反应生成NaOH、氯气和水反应生成HCl和HClO.
解答:
解:根据元素在周期表中的位置知,①②③④⑤⑥⑦⑧分别是C、N、O、Na、Al、S、Cl、Ar元素,
(1)稀有气体元素的原子最外层电子达到稳定结构,所以稀有气体的化学性质最不活泼,所以Ar是最不活泼的元素,Ar原子核外有3个电子层、最外层电子数是8,其原子结构示意图为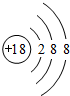 ,故答案为:
,故答案为: ;
;
(2)氯原子之间通过共用电子对形成氯气分子,其形成过程为: ,故答案为:
,故答案为: ;
;
(3)元素的非金属性越强,其最高价氧化物的水化物酸性越强(O、F元素除外),这些元素除了F、O元素外,非金属性最强的是Cl元素,则其最高价氧化物的水化物酸性最强的是HClO4;金属性越强的元素,其对应的最高价氧化物的水化物碱性越强,这些元素中,金属性最强的元素是Na元素,则其最高价氧化物的水化物碱性最强的是NaOH; Al(OH)3能和强酸、强碱反应生成盐和水,所以 Al(OH)3具有两性;
故答案为:HClO4;NaOH;Al(OH)3;
(4)元素③的氢化物是水,水分子中每个氢原子和氧原子之间形成共价键,其电子式为 ;钠和水反应生成NaOH,反应方程式为2Na+2H2O=2NaOH+H2↑,氯气和水反应生成HCl和HClO,反应方程式为Cl2+H2O=HCl+HClO;
;钠和水反应生成NaOH,反应方程式为2Na+2H2O=2NaOH+H2↑,氯气和水反应生成HCl和HClO,反应方程式为Cl2+H2O=HCl+HClO;
故答案为: ;2Na+2H2O=2NaOH+H2↑;Cl2+H2O=HCl+HClO.
;2Na+2H2O=2NaOH+H2↑;Cl2+H2O=HCl+HClO.
(1)稀有气体元素的原子最外层电子达到稳定结构,所以稀有气体的化学性质最不活泼,所以Ar是最不活泼的元素,Ar原子核外有3个电子层、最外层电子数是8,其原子结构示意图为
 ,故答案为:
,故答案为: ;
;(2)氯原子之间通过共用电子对形成氯气分子,其形成过程为:
 ,故答案为:
,故答案为: ;
;(3)元素的非金属性越强,其最高价氧化物的水化物酸性越强(O、F元素除外),这些元素除了F、O元素外,非金属性最强的是Cl元素,则其最高价氧化物的水化物酸性最强的是HClO4;金属性越强的元素,其对应的最高价氧化物的水化物碱性越强,这些元素中,金属性最强的元素是Na元素,则其最高价氧化物的水化物碱性最强的是NaOH; Al(OH)3能和强酸、强碱反应生成盐和水,所以 Al(OH)3具有两性;
故答案为:HClO4;NaOH;Al(OH)3;
(4)元素③的氢化物是水,水分子中每个氢原子和氧原子之间形成共价键,其电子式为
 ;钠和水反应生成NaOH,反应方程式为2Na+2H2O=2NaOH+H2↑,氯气和水反应生成HCl和HClO,反应方程式为Cl2+H2O=HCl+HClO;
;钠和水反应生成NaOH,反应方程式为2Na+2H2O=2NaOH+H2↑,氯气和水反应生成HCl和HClO,反应方程式为Cl2+H2O=HCl+HClO;故答案为:
 ;2Na+2H2O=2NaOH+H2↑;Cl2+H2O=HCl+HClO.
;2Na+2H2O=2NaOH+H2↑;Cl2+H2O=HCl+HClO.
点评:本题考查了元素周期表和元素周期律的应用,根据元素在周期表中的位置确定元素,再结合元素周期律来分析解答,熟练掌握元素周期律,并灵活运用知识解答,题目难度不大.

练习册系列答案
相关题目
下列离子方程式正确的是( )
| A、用Fe除去FeCl2溶液中的少量的FeCl3杂质:Fe+Fe3+=2Fe2+ | ||
B、实验室制取NO2:Cu+4H++2NO
| ||
C、硫酸溶液与氢氧化钡溶液混合:H++SO
| ||
D、向氯化铝溶液通足量氨气:Al3++4NH3+4H2O=4NH
|
现有A、B、C、D四种金属片,①把A、B用导线连接后同时浸入稀硫酸中,B上有气泡产生;②把C、D用导线连接后同时浸入稀硫酸中,C上发生还原反应;③把B、D用导线连接后同时浸入稀硫酸中,电子流动方向为:B→导线→D,则下列关于金属活动由强到弱顺序正确的是( )
| A、B>A>C>D |
| B、A>B>D>C |
| C、A>B>C>D |
| D、B>A>D>C |
已知A(g)+B(g)═C(g)△H1,D(g)+B(g)═E(g)△H2,且△H1<△H2.若A、D混合气体1mol完全与B反应,放热△H3,则A、D的物质的量之比为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列说法正确的是( )
A、
| ||
B、 互为同分异构体 互为同分异构体 | ||
| C、正丁烷与异丁烷互为同系物 | ||
| D、32S与33S是同种核素 |
 和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:I
和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:I

