题目内容
某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,实验小组利用A制备Al(OH)3的操作流程如下:
据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中分离溶液和沉淀所采取的操作名称是 ,该实验操作所用到的玻璃仪器有 .
(2)根据上述流程,写出D、E所含物质的化学式:沉淀D ;溶液E 、 .
(3)写出②、③反应的离子方程式:
② ;③ .

据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中分离溶液和沉淀所采取的操作名称是
(2)根据上述流程,写出D、E所含物质的化学式:沉淀D
(3)写出②、③反应的离子方程式:
②
考点:物质分离和提纯的方法和基本操作综合应用,制备实验方案的设计
专题:
分析:KAl(SO4)2溶于水,Al2O3和Fe2O3均不溶于水,混合物A加水溶解后,溶液中是KAl(SO4)2,沉淀C是Al2O3和Fe2O3;
向沉淀中加NaOH溶液,Fe2O3不反应,Al2O3可与NaOH溶液反应生成NaAlO2,向NaAlO2溶液中通入CO2可得Al(OH)3沉淀,滤液为碳酸氢钠;
向溶液中加过量氨水,溶液与过量氨水反应,Al3+被沉淀,得到氢氧化铝沉淀,溶液中剩余的是K2SO4 和(NH4)2SO4,经过蒸发、结晶,得到的是K2SO4 和(NH4)2SO4,故E为K2SO4 和(NH4)2SO4,以此来解答.
向沉淀中加NaOH溶液,Fe2O3不反应,Al2O3可与NaOH溶液反应生成NaAlO2,向NaAlO2溶液中通入CO2可得Al(OH)3沉淀,滤液为碳酸氢钠;
向溶液中加过量氨水,溶液与过量氨水反应,Al3+被沉淀,得到氢氧化铝沉淀,溶液中剩余的是K2SO4 和(NH4)2SO4,经过蒸发、结晶,得到的是K2SO4 和(NH4)2SO4,故E为K2SO4 和(NH4)2SO4,以此来解答.
解答:
解:KAl(SO4)2溶于水,Al2O3和Fe2O3均不溶于水,混合物A加水溶解后,溶液中是KAl(SO4)2,沉淀C是Al2O3和Fe2O3;
向沉淀中加NaOH溶液,Fe2O3不反应,Al2O3可与NaOH溶液反应生成NaAlO2,向NaAlO2溶液中通入CO2可得Al(OH)3沉淀,滤液为碳酸氢钠;
向溶液中加过量氨水,溶液与过量氨水反应,Al3+被沉淀,得到氢氧化铝沉淀,溶液中剩余的是K2SO4 和(NH4)2SO4,经过蒸发、结晶,得到的是K2SO4 和(NH4)2SO4,故E为K2SO4 和(NH4)2SO4,
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是过滤,该实验操作所用到的玻璃仪器有玻璃棒、烧杯、漏斗,
故答案为:过滤; 玻璃棒、烧杯、漏斗;
(2)由上述分析可知,B为Al2O3,D为Fe2O3,E为K2SO4和(NH4)2SO4,故答案为:Fe2O3;(NH4)2SO4、K2SO4;
(3)②、③反应的离子方程式分别为Al3++3NH3?H2O═Al(OH)3↓+3NH4+、AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-,
故答案为:Al3++3NH3?H2O═Al(OH)3↓+3NH4+;AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-.
向沉淀中加NaOH溶液,Fe2O3不反应,Al2O3可与NaOH溶液反应生成NaAlO2,向NaAlO2溶液中通入CO2可得Al(OH)3沉淀,滤液为碳酸氢钠;
向溶液中加过量氨水,溶液与过量氨水反应,Al3+被沉淀,得到氢氧化铝沉淀,溶液中剩余的是K2SO4 和(NH4)2SO4,经过蒸发、结晶,得到的是K2SO4 和(NH4)2SO4,故E为K2SO4 和(NH4)2SO4,
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是过滤,该实验操作所用到的玻璃仪器有玻璃棒、烧杯、漏斗,
故答案为:过滤; 玻璃棒、烧杯、漏斗;
(2)由上述分析可知,B为Al2O3,D为Fe2O3,E为K2SO4和(NH4)2SO4,故答案为:Fe2O3;(NH4)2SO4、K2SO4;
(3)②、③反应的离子方程式分别为Al3++3NH3?H2O═Al(OH)3↓+3NH4+、AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-,
故答案为:Al3++3NH3?H2O═Al(OH)3↓+3NH4+;AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-.
点评:本题考查混合物分离提纯方法的选择和应用,为高频考点,把握流程中发生的反应及混合物分离方法为解答的关键,侧重分析与实验能力的考查,注意氧化铝、氢氧化铝的两性,题目难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
A、常温下
| ||
| B、向碳酸氢钙溶液中加入过量氢氧化钠溶液发生反应的离子方程式可表示为:Ca2++HCO3-+OH-═CaCO3↓+H2O | ||
| C、加入铝能放出H2的溶液中一定能大量存在Cu2+、Na+、NO3-、C1?四种离子 | ||
| D、常温下将0.4 mol/L HB溶液和0.2 mol/L NaOH溶液等体积混合后溶液的pH=3,则混合溶液中离子浓度的大小顺序为:c(B-)>c(Na+)>c(H+)>c(OH-) |
溶液中的下列微粒体系,能够大量共存的是( )
| A、pH=1的溶液中:Fe2+、NO3-、Na+ |
| B、氨水中:Al3+、SO42-、Mg2+ |
| C、容器底部有硫粉:Fe3+、Cu2+、Cl- |
| D、NaNO3溶液中:Al3+、AlO2- |

 .化合物
.化合物 是合成抗癌药物美法伦的中间体,请写出以
是合成抗癌药物美法伦的中间体,请写出以 和
和 为原料制备该化合物的合成路线流程图(无机试剂任用).
为原料制备该化合物的合成路线流程图(无机试剂任用).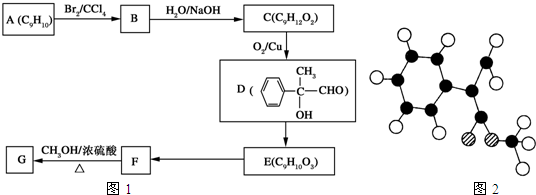
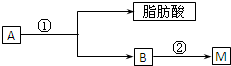
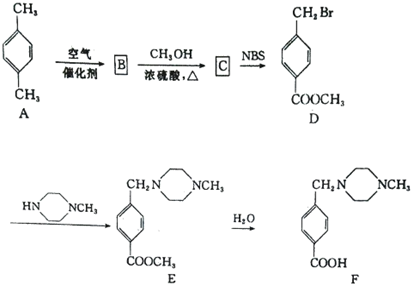
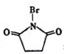 ,则反应C→D的化学方程式为
,则反应C→D的化学方程式为