题目内容
1.某溶液可能含有Clˉ、SO42ˉ、CO32ˉ、NH4+、Fe3+、Fe2+、Al3+ 和Na+.某同学为了确认其成分,取部分试液,设计并完成了如下实验:由此可知原溶液中( )
| A. | 原溶液中c(Fe3+)=0.2 mol•L-1 | |
| B. | 溶液中至少有4种离子存在,其中Clˉ一定存在,且c(Clˉ)≥0.2 mol•L-1 | |
| C. | SO42ˉ、NH4+、Na+一定存在,CO32ˉ、Al3+一定不存在 | |
| D. | 要确定原溶液中是否含有Fe2+,其操作为:取少量原溶液于试管中,加入足量酸性高锰酸钾溶液,若溶液紫红色褪去,则证明原溶液中有Fe2+ |
分析 加入过量NaOH溶液,加热,得到0.02mol气体,该气体为氨气,原溶液中一定存在0.02molNH4+;
产生的红褐色沉淀为氢氧化铁,1.6g固体为三氧化二铁,氧化铁的物质的量为0.01mol,则原溶液中含有0.02mol铁元素,可能为Fe3+、Fe2+,原溶液中一定没有CO32-;
滤液通入二氧化碳无现象,则原溶液中一定不存在Al3+;
4.66g不溶于盐酸的固体为硫酸钡,硫酸钡的物质的量为0.02mol,原溶液中含有0.02mol硫酸根离子;
颜色反应为黄色,则溶液中存在钠离子,由于加入了氢氧化钠溶液,无法判断原溶液中是否含有钠离子;
根据溶液电中性判断是否存在氯离子.
解答 解:加入过量NaOH溶液,加热,得到0.02mol气体,该气体为氨气,原溶液中一定存在0.02molNH4+;
产生的红褐色沉淀为氢氧化铁,1.6g固体为三氧化二铁,氧化铁的物质的量为0.01mol,则原溶液中含有0.02mol铁元素,可能为Fe3+、Fe2+,原溶液中一定没有CO32-;
滤液通入二氧化碳无现象,则原溶液中一定不存在Al3+;
颜色反应为黄色,则溶液中一定存在钠离子,由于加入了NaOH,无法判断原溶液中是否含有Na+;
4.66g不溶于盐酸的固体为硫酸钡,硫酸钡的物质的量为0.02mol,则原溶液中含有0.02mol硫酸根离子,
据电荷守恒,原溶液中一定有Cl-,物质的量至少为 0.02mol×2+0.02mol-0.02mol×2=0.02mol,
A.根据以上分析可知,原溶液中含有0.02mol铁元素,无法判断存在的是铁离子或者亚铁离子,故A错误;
B.根据以上分析,原溶液中一定存在0.02molNH4+,0.02molSO42-,0.02molFe3+、Fe2+中的一种,当铁元素全部为亚铁离子时,阳离子所带电荷的物质的量最小,所以正电荷物质的量最少为:0.02mol×2+0.02mol=0.06mol,而负电荷的物质的量为:0.02mol×2=0.04mol,根据溶液电中性可知,原溶液中一定存在Cl-,且c(Cl-)≥$\frac{0.06mol-0.04mol}{0.1L}$=0.2 mol•L-1,故B正确;
C.根据以上分析可知,原溶液中一定存在SO42-、NH4+、Cl-,只是存在Fe3+、Fe2+中的一种,其离子的物质的量为0.02mol,一定不存在CO32-、Al3+;由于第一步中加入了氢氧化钠溶液,引进了钠离子,无法确定原溶液中是否含有钠离子,故C错误;
D.加入高锰酸钾,如含由亚铁离子,则被氧化生成铁离子,由于高锰酸钾过量,则现象不明显,可用硫氰化亚铁铵检验,观察是否生成沉淀,故D错误;
故选B.
点评 本题考查物质分离、提纯实验方案的设计,为高频考点,把握实验流程中的试剂、发生的反应及分离方法为解答的关键,侧重分析能力、实验能力的综合考查,题目难度不大,注意根据溶液电中性判断氯离子存在的方法.

 阅读快车系列答案
阅读快车系列答案①SiO2→Na2SiO3 ②Fe(OH)2-→Fe(OH)3 ③SiO2→H2SiO3
④Al2O3-→Al(OH)3 ⑤Na2O2→NaCl ⑥Al→NaAlO2( )
| A. | ①② | B. | ③④ | C. | ②③ | D. | ⑤⑥ |
(1)已知:①4NH3(g)+3O2(g)═2N2(g)+6H2O(g)△H=-1266.8kJ•mol-1
②N2(g)+O2(g)═2NO(g)△H=180.5kJ•mol-1
写出氨高温催化氧化的热化学方程式4NH3(g)+5O2(g)$\frac{\underline{催化剂}}{△}$4NO(g)+6H2O(g)△H=-905.8KJ/mol.
(2)氨气、空气可以构成燃料电池,其电池反应原理为4NH3+3O2═2N2+6H2O.则原电解质溶液显碱性(填“酸性”、“中性”或“碱性”),负极的电极反应式为2NH3+6OH--6e-═N2+6H2O.
(3)合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:
| 温度/°C | 200 | 300 | 400 |
| K | 1.0 | 0.86 | 0.5 |
②理论上,为了增大平衡时H2的转化率,可采取的措施是ad(填字母序号);
a.增大压强 b.使用合适的催化剂
c.升高温度 d.及时分离出产物中的NH3
③400°C时,测得氨气、氮气、氢气的物质的量浓度分别为3mol•L-1、2mol•L-1、1mol•L-1时,此时刻该反应的v正(N2)<v逆(N2)(填“>”、“<”或“=”).
(4)①25°C时,将amol•L-1的氨水与0.1mol•L-1的盐酸等体积混合.当溶液中c(NH4+)=c(Cl-)时,用含a的代数式表示NH3•H2O的电离常数Kb=$\frac{1{0}^{-8}}{a-0.1}$;
②向25mL0.10mol•L-1的盐酸中滴加氨水至过量,该过程中离子浓度大小关系一定不正确的是d (填字母序号).
a.c(Cl-)>c(H+)>c(NH4+)>c(OH-) b.c(C1-)>c(NH4+)=c(H+)>c(OH-)
c.c(NH4+)>c(OH-)>c(Cl-)>c(H+) d.c(OH-)>c(NH4+)>c(H+)>c(Cl-)
| 选项 | 实验内容 | 实验现象 | 实验结论 |
| A | 将几滴水加入蔗糖中并搅拌,再加入浓硫酸,迅速搅拌 | 蔗糖逐渐变黑,体积膨胀,形成疏松多孔的物质 | 只体现了浓硫酸的脱水性 |
| B | 将铜片放入浓硝酸中 | 产生大量红棕色气体,溶液变为蓝绿色 | 体现了浓硝酸的强氧化性和酸性 |
| C | 溴乙烷和氢氧化钠溶液充分反应,用足量稀硝酸酸化,再加入硝酸银溶液 | 生成淡黄色沉淀 | 溴乙烷中含有溴元素 |
| D | 将溴水加入苯中并充分振荡 | 溴水褪色下层有机层为橙红色 | 苯与溴发生了萃取作用 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 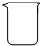 | B. | 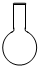 | C. | 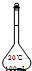 | D. |  |
| A. | 将饱和氯水滴到淀粉碘化钾试纸上,如果试纸先变蓝后变白,说明氯气具有氧化性和漂白性 | |
| B. | 向Na2S2O3稀溶液中加入稀硫酸,发生如下反应:S2O32-+2H+═SO2↑+S↓+H2O,利用产生浑浊的快慢或产生气泡的快慢可以测定该反应在不同条件下的反应速率 | |
| C. | 乙酸乙酯中少量乙醇杂质可加水除去,其原理与溴水中加四氯化碳萃取溴类似 | |
| D. | 将SO2通入品红溶液中,品红溶液褪色,加热褪色后的溶液,恢复红色,说明亚硫酸不稳定 |
| A. | 用湿润的pH试纸测稀碱液的pH,测定值偏小 | |
| B. | 滴定实验时,锥形瓶用蒸馏水洗净后,直接盛待测液 | |
| C. | 用洁净的玻璃棒蘸取新制氯水,滴在pH 试纸上,然后与比色卡对照,可测定新制氯水的pH 值 | |
| D. | 基于硫代硫酸钠与稀硫酸反应生成S和SO2,在定量测定反应速率时,既可用S对标记遮盖法,也可用排水法测SO2体积,计算出其的反应速率 |
| A. | 丙烯酸(CH2=CHCOOH)和山梨酸(CH3CH=CHCH=CHCOOH)不是同系物,它们与氢气充分反应后的产物也不是同系物 | |
| B. | 分子式为C7H16的有机物中有三种不同化学环境的氢原子,此有机物一定是2,4-二甲基戊烷或3,3-二甲基戊烷 | |
| C. | 完全燃烧等质量的甲醛、乙酸、葡萄糖、蔗糖消耗的氧气量相等 | |
| D. | 还原性染料靛蓝的结构简式为: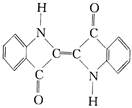 ,它的分子式是:C16H10N2O2 ,它的分子式是:C16H10N2O2 |