题目内容
用NA表示阿伏德罗常数,下列叙述正确的是( )
| A、标准状况下,22.4 L H2O含有的分子数为1 NA |
| B、100mL0.1mol/L Na2CO3溶液中含有的Na+离子数为0.1NA |
| C、通常状况下,NA个CO2分子占有的体积为22.4 L |
| D、48gO2和O3的混合气体中氧原子数目为3NA |
考点:阿伏加德罗常数
专题:
分析:A.标准状况下,水的状态不是气体,不能使用标况下的气体摩尔体积计算水的物质的量;
B.100mL0.1mol/L Na2CO3溶液中碳酸钠的物质的量为0.01mol,含有0.02mol钠离子;
C.气体摩尔体积22.4L/mol使用条件是标准状况;
D.根据O3和O2都由O原子构成分析.
B.100mL0.1mol/L Na2CO3溶液中碳酸钠的物质的量为0.01mol,含有0.02mol钠离子;
C.气体摩尔体积22.4L/mol使用条件是标准状况;
D.根据O3和O2都由O原子构成分析.
解答:
解:A.标况下,水不是气体,不能使用标况下的气体摩尔体积计算22.4L水的物质的量,故A错误;
B.100mL0.1mol/L Na2CO3溶液中碳酸钠的物质的量是0.01mol,0.01mol碳酸钠中含有0.02mol钠离子,含有的Na+离子数为0.02NA,故B错误;
C.不是标准状况,不能使用气体摩尔体积22.4L/mol,故C错误;
D.O3和O2都由O原子构成,则48gO3和O2的混合气体中含有的氧原子的物质的量为
=3mol,氧原子数为3NA,故D正确;
故选D.
B.100mL0.1mol/L Na2CO3溶液中碳酸钠的物质的量是0.01mol,0.01mol碳酸钠中含有0.02mol钠离子,含有的Na+离子数为0.02NA,故B错误;
C.不是标准状况,不能使用气体摩尔体积22.4L/mol,故C错误;
D.O3和O2都由O原子构成,则48gO3和O2的混合气体中含有的氧原子的物质的量为
| 48g |
| 16g/mol |
故选D.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,要求学生掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
室温下,下列各组离子或分子在指定分散系中能大量共存的是( )
| A、FeCl3溶液中:H+、Na+、Cl-、H2O2 | ||||
| B、酸性KMnO4的溶液中:Na+、NO3-、K+、CH3CH2OH | ||||
| C、混有氯化氢气体的氯气中:O2、CH4、N2、NH3 | ||||
D、c(H+)=0.10mol/L的溶液中:NH
|
下列说法正确的是( )
| A、需要加热方能发生的反应一定是吸热反应 |
| B、放热的反应在常温下一定很容易发生 |
| C、反应是放热还是吸热,取决于反应物和生成物所具有的总能量的相对大小 |
| D、伴有能量变化的物质变化都是化学变化 |
下列仪器的使用、记录的数据或实验的结论正确的是( )
| A、用25mL量筒量取22.30mL盐酸 |
| B、用托盘天平称量8.75g食盐 |
| C、将20gNa2CO3溶于80g水中制得20%的Na2CO3溶液 |
| D、将标准状况下22.4LHCl气体溶于1L水中可制得1mol/L盐酸 |
化学与资源、环境、生活关系密切,下列说法错误的是( )
| A、维生素C具有还原性,在人体内起抗氧化作用 |
| B、新型氢动力计程车可以降低PM2.5的排放,减少大气污染 |
| C、碘是人体必需微量元素,所以要多吃富含高碘酸的食物 |
| D、高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱溶液会“断路” |
如图所示, 为直流电源,
为直流电源, 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀槽.接通电路(未闭合K)后发现
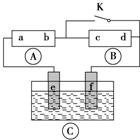
为电镀槽.接通电路(未闭合K)后发现 上的c点显红色.为实现铁上镀铜,使c、d两点短路.下列叙述不正确的是( )
上的c点显红色.为实现铁上镀铜,使c、d两点短路.下列叙述不正确的是( )
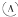 为直流电源,
为直流电源,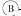 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀槽.接通电路(未闭合K)后发现
为电镀槽.接通电路(未闭合K)后发现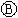 上的c点显红色.为实现铁上镀铜,使c、d两点短路.下列叙述不正确的是( )
上的c点显红色.为实现铁上镀铜,使c、d两点短路.下列叙述不正确的是( ) 
| A、b为直流电源的负极 |
| B、f极为阴极,发生还原反应 |
| C、e极材料为铁片,f极材料的铜片 |
| D、可选用CuSO4溶液或CuCl2溶液作电镀液 |
