题目内容
20.白色粉末由Na2S、Na2SO3、Na2S2O3、Na2S04和NaCl等物质中的三种混合而成.取一定量A样品投入100mL2.2mol/L盐酸中,充分反应后过滤,最终得到100mLpH=0的溶液,将此滤液蒸干,又得到8.19g纯净物B.(1)B的化学式为NaCl;
(2)请通过计算推断A中是否含有NaCl?
(3)若反应中还生成V升(标准状况)气体,且该气体不会使品红溶液褪色,则取出的A样品中肯定含有Na2S(0.04-$\frac{V}{15.8}$)mol(用含V的代数式表示);
(4)A中各组分的物质的量比不同时,所产生的沉淀的量也不同.上述A样品与盐酸反应可生成沉淀的质量最大值为2.56g.
分析 (1)A样品与盐酸反应,Na2S、Na2SO3、Na2S2O3会反应生成NaCl,由蒸干滤液后一定含有NaCl,最后得到8.19g纯净物B,则说明原样品A中没有Na2SO4,B是NaCl;
(2)100 mL 2.2 mol/L的盐酸反应后最终得到100mLpH=0的溶液,则HCl有剩余,则消耗HCl为0.1L×2.2mol/L-0.1L×1.0mol/L=0.12mol,可知生成的NaCl为0.12mol,故生成NaCl的质量=0.12mol×58.5g.mol=7.02 g<8.19g,可知样品A中必定有NaCl;
(3)反应生成的气体不能使品红溶液褪色,则为H2S,根据Na2S+2HCl=2NaCl+H2S↑计算该反应生成消耗HCl物质的量、Na2S的物质的量;
由于样品A由三种混合而成,则A组成情况可能为:①A为Na2S、Na2SO3和NaCl混合,②A为Na2S、Na2S2O3和NaCl混合,计算Na2S、Na2SO3(或Na2S2O3)共同与盐酸反应时应消耗HCl的物质的量,由2Na2S+Na2SO3+6HCl=6NaCl+3S↓+3H2O,2Na2S+Na2S2O3+6HCl=6NaCl+4S↓+3H2O,可知Na2S~3HCl,进而计算该反应中Na2S的物质的量;
(4)由钠离子守恒,则Na2S、Na2SO3(或Na2S2O3)的总物质的量为$\frac{0.12mol}{2}$=0.06mol,恰好发生反应:2Na2S+Na2S2O3+6HCl=6NaCl+4S↓+3H2O,化合物中S元素全部转化为S单质时得到沉淀量最大.
解答 解:(1)A样品与盐酸反应,Na2S、Na2SO3、Na2S2O3会反应生成NaCl,由蒸干滤液后一定含有NaCl,最后得到8.19g纯净物B,则说明原样品A中没有Na2SO4,B是NaCl,
故答案为:NaCl;
(2)100 mL 2.2 mol/L的盐酸反应后最终得到100mLpH=0的溶液,则HCl有剩余,则消耗HCl为0.1L×2.2mol/L-0.1L×1.0mol/L=0.12mol,可知生成的NaCl为0.12mol,故生成NaCl的质量=0.12mol×58.5g.mol=7.02 g<8.19g,可知样品A中必定有NaCl,
答:A中含有NaCl;
(3)反应生成的气体不能使品红溶液褪色,则为H2S,
Na2S+2HCl=2NaCl+H2S↑
1 mol 2 mol 22.4 L
n′(Na2S) n(HCl) VL
则n′(Na2S)=$\frac{VL×1mol}{22.4L}$=$\frac{V}{22.4}$mol
n(HCl)=$\frac{VL×2mol}{22.4L}$=$\frac{V}{11.2}$mol
而整个过程实际参加反应的HCl为0.12 mol,
由于样品A由三种混合而成,则A组成情况可能为:①A为Na2S、Na2SO3和NaCl混合,②A为Na2S、Na2S2O3和NaCl混合,
由2Na2S+Na2SO3+6HCl=6NaCl+3S↓+3H2O,2Na2S+Na2S2O3+6HCl=6NaCl+4S↓+3H2O,可知Na2S~3HCl,故n″(Na2S)=$\frac{1}{3}$(0.12-$\frac{V}{11.2}$)mol,
则n(Na2S)=n′(Na2S)+n″(Na2S)=$\frac{V}{22.4}$mol+$\frac{1}{3}$(0.12-$\frac{V}{11.2}$)mol=(0.04-$\frac{V}{15.8}$)mol,
故答案为:(0.04-$\frac{V}{15.8}$);
(4)由钠离子守恒,则Na2S、Na2SO3(或Na2S2O3)的总物质的量为$\frac{0.12mol}{2}$=0.06mol,恰好发生反应:2Na2S+Na2S2O3+6HCl=6NaCl+4S↓+3H2O,化合物中S元素全部转化为S单质时得到沉淀量最大,此时Na2S、Na2S2O3的物质的之比为2:1,物质的量分别为0.04mol、0.02mol,则生成S为0.08mol,生成S的最大质量为0.08×32g/mol=2.56g,
故答案为:2.56g.
点评 本题考查混合物的计算,关键是明确发生的反应,侧重考查学生的分析计算能力,(3)(4)为易错点、难点,注意计算混合物的总物质的量,题目难度较大.

| 紫铜 | 青铜 | 铜绿 | |
| 主要成分 | 纯铜 | 铜锡合金 | Cu2(OH)2CO3 |
| 性质与用途 | 紫红色,质软,导电性能良好;主要用作电线电缆. | 多呈灰绿色,熔点低、硬度大、可塑性强;可铸造成各种器具. | 不溶于水的灰绿色粉末,溶于酸,加热易分解;可作颜料、杀虫剂. |
【猜想假设】
(1)小吴同学认为可能是纯铜制品表面涂上了灰绿色的油漆;
小周同学认为可能是青铜(铜锡合金),因为常见的青铜是灰绿色的;
小黄同学认为是纯铜制品,只是表面长出了铜绿[Cu2(OH)2CO3];
除上述猜想外,其他合理的猜想是青铜表面长出了铜绿(只写一个).
【实验验证】三位同学为了验证各自上述的猜想,进行了以下探究:
(2)小吴刮下部分灰绿色物质放入燃烧匙中进行灼烧,发现该物质不能燃烧,证明灰绿色物质不是油漆.其判断依据是油漆是有机物,可燃.
(3)小周刮下足量的灰绿色物质投入盐酸溶液中,观察到有气体产生,实验表明该气体不能燃烧.将表面刮净后的铜制品也投入盐酸中,并无气体产生.由此证明该铜制品不是青铜,理由是青铜中含有金属锡,能与盐酸反应生成氢气.
(4)根据上述实验,小黄认为灰绿色物质可能是铜绿[Cu2(OH)2CO3].于是按如图所示装置进行实验.

实验证明小黄的猜测是正确的,因为在A中观察到灰绿色物质变黑,B中观察到了白色固体变蓝色的现象,C中观察到了澄清石灰水变浑浊的现象.
B中所发生反应的化学方程式为:CuSO4+5H2O=CuSO4•5H2O.
如果将实验装置中的B和C进行调换,将无法得出灰绿色物质是铜绿的结论,原因是无法确定分解产物中是否有水.
【实验拓展】
(5)小黄同学还从网上找到了利用氨水擦拭去除铜绿的方法,其原理是氨水与碱式碳酸铜反应生成铜氨络离子[Cu(NH3)42+],其离子方程式可表示为:Cu2(OH)2CO3+8NH3•H2O=2Cu(NH3)42++2OH-+CO32-+8H2O.
| A. | B与A只能组成BA3化合物 | |
| B. | C、D、E形成的化合物与稀硫酸可能发生氧化还原反应 | |
| C. | A、B、C形成的化合物一定不能发生水解 | |
| D. | E的氧化物对应的水化物一定有强的氧化性 |
| 操作 | 现象 | 结论 | |
| A | 向试管中的无色溶液内滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口 | 试纸不变蓝 | 不能确定原溶液中是否含有NH4+ |
| B | 加热盛有铜与浓硫酸的试管,发现试管底部出现白色固体,直接向试管中加入适量水 | 白色固体溶解,溶液变蓝色 | 白色固体为无水硫酸铜 |
| C | 将稀硫酸酸化的H2O2溶液滴入FeCl2溶液中 | 溶液变黄色 | 氧化性:H2O2>Fe3+ |
| D | 向蔗糖中加入浓硫酸,并不断用玻璃棒搅拌 | 变黑,体积膨胀,放出刺激性气体 | 浓硫酸具有脱水性和强氧化性,反应中生成C、SO2和CO2等 |
| A. | A | B. | B | C. | C | D. | D |
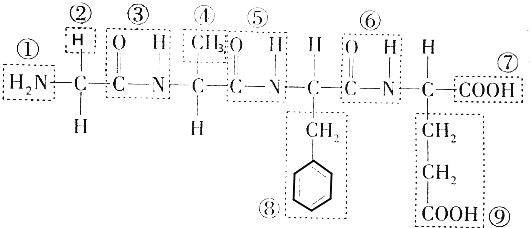
| A. | 能发生脂化反应的酸一定是羧酸 | |
| B. | 蛋白质溶液中加入浓Na2SO4溶液,蛋白质从溶液中凝聚而析出叫盐析 | |
| C. | 天然蛋白质一定条件下水解的最终产物是α-氨基酸 | |
| D. | 淀粉、纤维素和油脂在一定条件下都能发生水解反应 |
| Y | ||||
| Q | W | X | Z |
(1)Y的原子结构示意图为
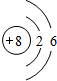 ;举一例说明Z的非金属性比X的非金属性强的事实:酸性强弱;HClO4>H3PO4,或稳定性:HCl>PH3.
;举一例说明Z的非金属性比X的非金属性强的事实:酸性强弱;HClO4>H3PO4,或稳定性:HCl>PH3.(2)W、X、Y的原子半径由大到小依次是(填元素符号)r(Si)>r(P)>r(O);W与Z形成的化合物电子式为
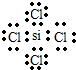 .
.(3)将Z的单质通入到含等物质的量FeBr2溶液中充分反应的离子方程式为2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-.
(4)已知:2Na(s)+1/2Y2(g)=Na2Y(s)△H=-414kJ/mol;2Na(s)+Y2(g)═Na2Y2(s)△H=-511kJ/mol;则Na2Y(s) 转变为Na2Y2(s)的反应一定条件下能自发进行的理由是Na2O(s)+$\frac{1}{2}$O2(g)=Na2O2(s)△H=-97 kJ/mol,而△S<0,△H-T△S在低温下小于0,可自发进行.
将0.2mol Na2Y2加入到100mL1mol/L QZ3中,充分反应的化学方程式为2Na2O2+AlCl3=NaAlO2+3NaCl+O2↑.
(5)R与W同周期,已知:在T℃时Ksp[R(OH)2]的值为4.0×l0-12,则R(OH)2饱和溶液中c(OH-)=2.0×l0-4 mol•L-1.
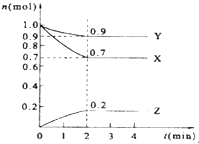 某温度时,在2L的密闭容器中,X、Y、Z三种气体物质的量随时间的变化曲线如图所示.
某温度时,在2L的密闭容器中,X、Y、Z三种气体物质的量随时间的变化曲线如图所示.