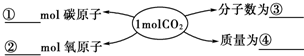
题目内容
1molFe2+与足量的H2O2溶液反应,转移2nA个电子 (判断对错)
考点:化学方程式的有关计算
专题:计算题
分析:Fe2+与足量的H2O2溶液反应,H2O2+2Fe2++2H+=2Fe3++2H2O,1mol Fe2+被氧化成1mol Fe3+,失去1mol电子,据此分析解答.
解答:
解:过氧化氢中氧的化合价为-1价,Fe2+具有还原性,两者反应过氧化氢中的氧元素化合价降为-2价,发生反应H2O2+2Fe2++2H+=2Fe3++2H2O,1mol Fe2+被氧化成1mol Fe3+,失去1mol电子,转移N=n×NA=NA个电子,
故答案为:错误;
故答案为:错误;
点评:本题考查了过氧化氢的氧化性,过氧化氢中的氧元素化合价从-1价降为-2价为解答的关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
实验室在配制Fe2(SO4)3水溶液时,先把Fe2(SO4)3晶体溶解在较浓H2SO4中,再加水稀释至所需浓度,如此操作的目的是( )
| A、防止硫酸铁分解 |
| B、抑制Fe2(SO4)3水解 |
| C、提高硫酸铁的溶解度 |
| D、提高溶液的pH |
对于醋酸溶液的下列说法中,不正确的是( )
| A、醋酸溶液中离子浓度的关系满足:c(H+)═c(OH-)+c(CH3COO-) |
| B、醋酸溶液中加入少量醋酸钠晶体,醋酸电离程度减小 |
| C、0.1mol/L的醋酸溶液中加水稀释,溶液中c(OH-)减小 |
| D、常温下,pH=3的醋酸溶液与pH=11的烧碱溶液等体积混合后,溶液中c(H+)<c(OH-) |
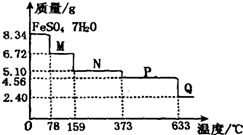 取8.34g FeS04?7H20样品加热,其受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示,则下列叙述中不正确的是( )
取8.34g FeS04?7H20样品加热,其受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示,则下列叙述中不正确的是( )| A、温度为78℃时固体物质M的化学式为FeSO4?4H2O | ||||
| B、温度为l59℃时固体物质N的化学式为FeSO4?H2O | ||||
C、在隔绝空气条件下,N得到P的化学方程式为:FeSO4
| ||||
| D、固体P隔绝空气加热至650℃,得到一种固体物质Q,同时有三种无色气体生成,Q的化学式为Fe2O3 |
下列实验操作或装置符合实验要求的是( )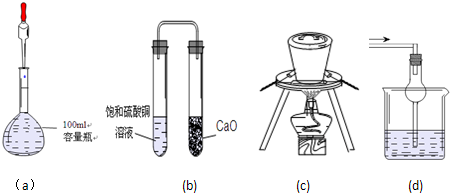

| A、(a) 可用于定容并量取15.00 mL NaOH溶液 |
| B、(b)装置放置一段时间后,饱和CuSO4溶液中出现蓝色晶体 |
| C、(c)可用于高温煅烧石灰石 |
| D、(d)可用于易溶于水的尾气吸收 |
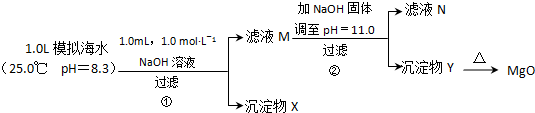
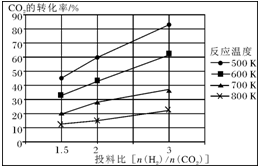 燃煤废气中的氮氧化物(NOx)、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等.
燃煤废气中的氮氧化物(NOx)、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等.