题目内容
13.据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇已成为现实,其反应方程如下:2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g).下列叙述错误的是( )| A. | 使用合适的催化剂可大大提高生产效率 | |
| B. | 由反应需在300℃进行,可知该反应是吸热反应 | |
| C. | 增大原料气中CO2的百分含量,可以提高H2的转化率 | |
| D. | 70MPa的压力,不仅可以增加单位时间内的产出,还可以提高CO2和H2的利用率 |
分析 根据催化剂、温度、浓度对化学反应速率和化学平衡的影响来分析解答,并注意吸热反应与反应的条件无关,
A.催化剂能提高化学反应速率,缩短达到平衡的时间;
B.反应需在300℃进行是为了获得较快的反应速率,催化剂活性大;
C.两种反应物增大一种物质的量会提高另一种物质转化率,本身转化率降低;
D.反应前后是气体体积减小的反应,增大压强平衡正向进行.
解答 解:A.因催化剂能提高化学反应速率,加快反应进行,则在一定时间内提高了生产效率,故A正确;
B.反应需在300℃进行是为了获得较快的反应速率,不能说明反应是吸热还是放热,故B错误;
C.充入大量CO2气体,能使平衡正向移动,提高H2的转化率,故C正确;
D.从平衡混合物中及时分离出产物,使平衡正向移动,可提高CO2和H2的转化率,故D正确;
故选B.
点评 本题考查化学反应速率和化学平衡知识,易错点为利用化学平衡知识判断反应吸热还是放热时,一定要注意温度的变化使反应正向移动还是逆向移动,倘若给出的信息为温度条件则无法判断,升高温度化学平衡向吸热的方向移动,而吸热反应取决于反应物与生成物总能量的相对大小,题目难度中等.

练习册系列答案
相关题目
4.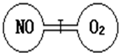 如图所示,两个连通容器用活塞分开,左右两室(体积相同)各充入一定量NO和O2,且恰好使两容器内气体密度相同.已知2NO+O2═2NO2,打开活塞,使NO与O2充分反应,则下列说法错误的是( )
如图所示,两个连通容器用活塞分开,左右两室(体积相同)各充入一定量NO和O2,且恰好使两容器内气体密度相同.已知2NO+O2═2NO2,打开活塞,使NO与O2充分反应,则下列说法错误的是( )
 如图所示,两个连通容器用活塞分开,左右两室(体积相同)各充入一定量NO和O2,且恰好使两容器内气体密度相同.已知2NO+O2═2NO2,打开活塞,使NO与O2充分反应,则下列说法错误的是( )
如图所示,两个连通容器用活塞分开,左右两室(体积相同)各充入一定量NO和O2,且恰好使两容器内气体密度相同.已知2NO+O2═2NO2,打开活塞,使NO与O2充分反应,则下列说法错误的是( )| A. | 开始时左右两室分子数相同 | B. | 反应开始后NO室压强减小 | ||
| C. | 最终容器内密度与原来相同 | D. | 最终容器内仍然有O2存在 |
1.对下列由电极和电解质溶液构成的装置叙述不正确的是( )
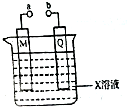

| A. | 若X、M、Q分别是H2SO4、Pb和PbO2,a、b连接后两极都有PbSO4生成 | |
| B. | 若X、M、Q分别是滴加酚酞的Na2SO4、C和Fe,a、b分别连接电源的正、负极,则通电后Q周围溶液颜色变红 | |
| C. | 若X、M、Q分别CuSO4、Cu和Fe,a、b分别连接电源的正、,则可在铁上镀铜 | |
| D. | 若X、M、Q分别是NaCl、C和Fe,则a、b连接后,M电极上有气体产生 |
8. 常温下,将Cl2缓慢通入水中至饱和,然后向其中滴加0.1mol/LKOH溶液.整个实验过程溶液中c(OH-)的变化曲线如图所示,不考虑次氯酸分解,下列叙述正确的是( )
常温下,将Cl2缓慢通入水中至饱和,然后向其中滴加0.1mol/LKOH溶液.整个实验过程溶液中c(OH-)的变化曲线如图所示,不考虑次氯酸分解,下列叙述正确的是( )
 常温下,将Cl2缓慢通入水中至饱和,然后向其中滴加0.1mol/LKOH溶液.整个实验过程溶液中c(OH-)的变化曲线如图所示,不考虑次氯酸分解,下列叙述正确的是( )
常温下,将Cl2缓慢通入水中至饱和,然后向其中滴加0.1mol/LKOH溶液.整个实验过程溶液中c(OH-)的变化曲线如图所示,不考虑次氯酸分解,下列叙述正确的是( )| A. | a点对应溶液中含有的分子有H2O、HClO、HCl、Cl2 | |
| B. | b点对应溶液中:c(H+)>c(Cl-)>c(HClO)>c(ClO-)>c(OH-) | |
| C. | c点对应溶液中:c(K+)=c(Cl-)+c(ClO-)+c(HClO) | |
| D. | 实验过程中可以用pH试纸测定溶液的pH |
5.在pH=x某电解质溶液中,插入两支惰性电极通直流电一段时间后,溶液的pH>x,则该电解质可能是( )
| A. | K2SO4 | B. | H2SO4 | C. | Ba(OH)2 | D. | AgNO3 |
20.下列说法正确的是( )
| A. | “纳米碳”属于“纳米材料”,若将纳米碳均匀地分散到蒸馏水中,所形成的物质能透过滤纸,不能透过半透膜,静置后会析出黑色沉淀 | |
| B. | 维生素C又称“抗坏血酸”,在人体内有重要的功能,是因为维生素C具有氧化性 | |
| C. | 表面打磨过的铝箔,在空气中加热至熔化也不滴落是因为表面生成了熔点很高的氧化铝薄膜包裹在铝的外面 | |
| D. | 氨很容易液化,液化时放热,液化后得到氨水 |
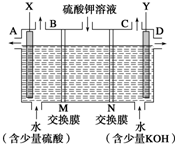 某小组同学设想用如图装置电解硫酸钾溶液来制取氧气、氢气、硫酸和氢氧化钾.
某小组同学设想用如图装置电解硫酸钾溶液来制取氧气、氢气、硫酸和氢氧化钾.