题目内容
3.简要回答下列问题:(1)误食重金属盐引起中毒,常服用牛奶解毒,这是因为牛奶中的蛋白质与重金属离子作用,从而减弱或消除重金属离子对人体的伤害
(2)不宜用铝制容器长时间盛装酸菜的原因是酸与铝表面的氧化膜反应,使金属溶解
(3)塑料制品垃圾造成的“白色污染”已成为社会的一大公害,请你提出一项治理“白色污染”的有效措施减少或不使用塑料袋.
分析 (1)重金属盐中毒是使人体内的蛋白质失去生理活性据此进行解答;
(2)酸能够与铝、氧化铝反应生成可溶性铝盐,铝摄入过多对人体有害;
(3)由于塑料难于降解,容易造成白色污染,治理“白色污染”可以从减少塑料袋使用入手或者使用可降解塑料代替.
解答 解:(1)重金属盐中毒是使人体内的蛋白质失去生理活性,牛奶的主要成分是蛋白质,所以人误食重金属盐中毒后,可迅速服用大量牛奶,牛奶中的蛋白质与重金属离子作用,从而减弱或消除重金属离子对人体的伤害;
故答案为:牛奶中的蛋白质与重金属离子作用,从而减弱或消除重金属离子对人体的伤害;
(2)不宜用铝制容器长时间盛装酸菜的原因:酸与铝表面的氧化膜反应,使金属溶解,铝摄入过多对人体有害;
故答案为:酸与铝表面的氧化膜反应,使金属溶解;
(3)理“白色污染”的有效措施:减少或不使用塑料袋或者使用可降解塑料代替,故答案为:减少或不使用塑料袋或者使用可降解塑料代替.
点评 本题考查了生活中常见的化学知识,熟悉蛋白质、铝、氧化性的性质,明确白色污染的根源是解题关键,题目难度不大.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
13.下列关于元素周期表和元素周期律的说法错误的是( )
| A. | Li、Na、K元素的原子核外电子层数随着核电荷数的增加而增多 | |
| B. | 第2周期元素从Li到F,得电子能力逐渐增强 | |
| C. | 元素原子的最外层电子数等于元素的最高正化合价 | |
| D. | O与S为同主族元素,且O比S的得电子能力强 |
11.阿司匹林的结构简式为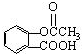 ,关于阿司匹林的叙述正确的是( )
,关于阿司匹林的叙述正确的是( )
 ,关于阿司匹林的叙述正确的是( )
,关于阿司匹林的叙述正确的是( )| A. | 阿司匹林属于抗生素 | |
| B. | 阿司匹林不能发生水解反应 | |
| C. | 阿司匹林具有解热镇痛作用 | |
| D. | 阿司匹林之所以成为经典药物是因为服用该药物没有不良反应 |
18.下列说法不正确的是( )
| A. | 磷酸的摩尔质量与阿伏加德罗常数(NA)个磷酸分子的质量在数值上相等 | |
| B. | 常温常压下,0.5NA个CO分子所占体积是11.2L | |
| C. | 1molNH4+中含有的电子数为10NA | |
| D. | 1L0.3mol/L的Na2SO4溶液中,含有Na+和 SO42-总数为0.9 NA |
8.以下是人们对原子结构的认识所经历的几个重要历史阶段:
①道尔顿提出的原子论;②汤姆孙提出的葡萄干面包原子模型;
③古希腊哲学家德谟克里特的古典原子论;④卢瑟福的原子结构行星模型.
其中先后顺序正确的是( )
①道尔顿提出的原子论;②汤姆孙提出的葡萄干面包原子模型;
③古希腊哲学家德谟克里特的古典原子论;④卢瑟福的原子结构行星模型.
其中先后顺序正确的是( )
| A. | ①③②④ | B. | ③②①④ | C. | ③①④② | D. | ③①②④ |
15.实验室从海带灰中提取碘的操作过程中,仪器选用不正确的是( )
| A. | 称取5 g左右的干海带--托盘天平 | |
| B. | 过滤煮沸后的海带灰和水的混合物--漏斗 | |
| C. | 用蒸发结晶的方法从氧化后的海带灰浸取液中提取碘--蒸发皿 | |
| D. | 用四氯化碳从氧化后的海带灰浸取液中提取碘--长颈漏斗 |
12.下列叙述中正确的是( )
| A. | 非金属氧化物都是酸性氧化物 | |
| B. | CaCO3是电解质,但CaCO3的水溶液几乎不导电 | |
| C. | 金属Al是非电解质,但金属Al能导电 | |
| D. | H2SO4(纯)是电解质,因此H2SO4(纯)能导电 |
13.下列各组物质中化学键的类型相同的是( )
| A. | HCl MgCl2 NH4Cl | B. | H2O Na2O CO2 | ||
| C. | CaCl2 NaOH H2O | D. | NH3 H2O CO2 |