题目内容
将两份等质量的铁粉,分别放入各100mL等物质的量浓度的稀盐酸和稀硫酸,充分反应后,生成氢气的体积比为3:4,若将铁粉与硫酸反应后的溶液稀释到200mL,测得溶液的pH=1,求:
(1)盐酸的物质的量浓度;
(2)标准状况下,铁与稀硫酸产生的氢气的体积.
(1)盐酸的物质的量浓度;
(2)标准状况下,铁与稀硫酸产生的氢气的体积.
考点:化学方程式的有关计算
专题:计算题
分析:将两份等质量的铁粉,分别放入各100mL等物质的量浓度的稀盐酸和稀硫酸,若酸都足量,则生成氢气的体积相等,若酸都不足量,由于n(HCl)=n(H2SO4),结合反应:Fe+2HCl=FeCl2+H2↑、Fe+H2SO4=FeSO4+H2↑,可知生成氢气体积之比为1:2,而实际两反应得到氢气体积之比为3:4,且将铁粉与硫酸反应后的溶液稀释到200mL,测得溶液的pH=1,说明HCl不足,而硫酸过量,
(1)令盐酸、硫酸的浓度为cmol/L,表示出n(HCl)、n(H2SO4),进而表示各自生成氢气的物质的量,结合二者生成氢气的体积之比列方程计算
(2)结合(1)的计算数据计算氢气的物质的量,再根据V=nVm计算氢气的体积.
(1)令盐酸、硫酸的浓度为cmol/L,表示出n(HCl)、n(H2SO4),进而表示各自生成氢气的物质的量,结合二者生成氢气的体积之比列方程计算
(2)结合(1)的计算数据计算氢气的物质的量,再根据V=nVm计算氢气的体积.
解答:
解:将两份等质量的铁粉,分别放入各100mL等物质的量浓度的稀盐酸和稀硫酸,若酸都足量,则生成氢气的体积相等,若酸都不足量,由于n(HCl)=n(H2SO4),结合反应:Fe+2HCl=FeCl2+H2↑、Fe+H2SO4=FeSO4+H2↑,可知生成氢气体积之比为1:2,而实际两反应得到氢气体积之比为3:4,且将铁粉与硫酸反应后的溶液稀释到200mL,测得溶液的pH=1,说明HCl不足,而硫酸过量,
(1)令盐酸、硫酸的浓度为cmol/L,则n(HCl)=n(H2SO4)=0.1L×cmol/L=0.1c mol,
由Fe+2HCl=FeCl2+H2↑可知,盐酸完全反应生成氢气为0.1cmol×
=0.05c mol,
若将铁粉与硫酸反应后的溶液稀释到200mL,测得溶液的pH=1,则n反应(H2SO4)=0.1c mol-
×0.2L××0.1mol/L=(0.1c-0.01)mol,由Fe+H2SO4=FeSO4+H2↑,可知硫酸反应生成氢气为(0.1c-0.01)mol,
充分反应后,生成氢气的体积比为3:4,则0.05c mol:(0.1c-0.01)mol=3:4,解得c=0.3,
答:盐酸的物质的量浓度为0.3mol/L.
(2)Fe与硫酸反应生成氢气的物质的量=(0.1c-0.01)mol=(0.1×0.3-0.01)mol=0.02mol,故标况下,生成氢气的体积=0.02mol×22.4L/mol=0.448L,
答:铁与硫酸反应生成氢气的体积为0.448L.
(1)令盐酸、硫酸的浓度为cmol/L,则n(HCl)=n(H2SO4)=0.1L×cmol/L=0.1c mol,
由Fe+2HCl=FeCl2+H2↑可知,盐酸完全反应生成氢气为0.1cmol×
| 1 |
| 2 |
若将铁粉与硫酸反应后的溶液稀释到200mL,测得溶液的pH=1,则n反应(H2SO4)=0.1c mol-
| 1 |
| 2 |
充分反应后,生成氢气的体积比为3:4,则0.05c mol:(0.1c-0.01)mol=3:4,解得c=0.3,
答:盐酸的物质的量浓度为0.3mol/L.
(2)Fe与硫酸反应生成氢气的物质的量=(0.1c-0.01)mol=(0.1×0.3-0.01)mol=0.02mol,故标况下,生成氢气的体积=0.02mol×22.4L/mol=0.448L,
答:铁与硫酸反应生成氢气的体积为0.448L.
点评:本题考化学方程式的有关计算,题目难度中等,注意根据反应的气体的体积关系判断过量问题是解答的关键.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
下列物质中,不能与金属钠反应放出氢气的是( )
| A、苯 | B、水 | C、乙醇 | D、乙酸 |
油酸的结构简式为CH3(CH2)7CH=CH(CH2)7COOH,下列说法正确的是( )
| A、油酸的分子式为C18H33O2 |
| B、油酸是乙酸的同系物 |
| C、油酸可与氢气发生加成反应 |
| D、1mol油酸最多可与1mol甘油酯化 |

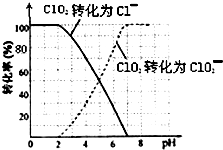 二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂.比Cl2更好.
二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂.比Cl2更好. 如图是某硫酸试剂瓶标签上的内容:
如图是某硫酸试剂瓶标签上的内容: