题目内容
下列有关化学用语使用正确的是( )
A、CH4分子的比例模型: |
B、NH3的电子式: |
C、硫离子的离子结构示意图: |
D、聚乙烯的结构简式为: |
考点:电子式、化学式或化学符号及名称的综合,原子结构示意图,球棍模型与比例模型
专题:
分析:A.根据甲烷的比例模型与球棍模型的表示方法判断;
B.漏掉了氮原子的1对孤电子对;
C.硫离子的核电荷数为16、核外电子总数为18;
D.聚乙烯的结构单元的主链含有2个C.
B.漏掉了氮原子的1对孤电子对;
C.硫离子的核电荷数为16、核外电子总数为18;
D.聚乙烯的结构单元的主链含有2个C.
解答:
解:A.甲烷为正面体结构,由原子相对大小表示空间结构为比例模型,则CH4分子的比例模型为 ,故A错误;
,故A错误;
B.氨气为共价化合物,分子中存在3对共用电子对,氮原子最外层为8个电子,氨气正确的电子式为: ,故B错误;
,故B错误;
C.硫离子的核电荷数为16,最外层达到8电子稳定结构,硫离子的离子结构示意图为: ,故C正确;
,故C正确;
D.乙烯发生加成反应生成聚乙烯,聚乙烯中不含双键,则聚乙烯的结构简式为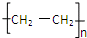 ,故D错误;
,故D错误;
故选C.
 ,故A错误;
,故A错误;B.氨气为共价化合物,分子中存在3对共用电子对,氮原子最外层为8个电子,氨气正确的电子式为:
 ,故B错误;
,故B错误;C.硫离子的核电荷数为16,最外层达到8电子稳定结构,硫离子的离子结构示意图为:
 ,故C正确;
,故C正确;D.乙烯发生加成反应生成聚乙烯,聚乙烯中不含双键,则聚乙烯的结构简式为
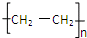 ,故D错误;
,故D错误;故选C.
点评:本题考查了常见化学用语的判断,题目难度中等,注意掌握比例模型与球棍模型、离子结构示意图与原子结构示意图、电子式等化学用语的概念及书写原则.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目
下列说法中,不正确的是( )
| A、若反应中形成化学键释放的能量大于断裂化学键所吸收的能量,则是放热反应 |
| B、若反应物的能量大于生成物的能量,则是放热反应 |
| C、化学反应中能量变化的大小与反应物的质量多少无关 |
| D、化学反应必然伴随着能量的变化和化学键的变化 |
元素X原子的最外层有3个电子,元素Y原子的最外层有6个电子,这两种元素形成的化合物的化学式可能是( )
| A、XY2 |
| B、X2Y3 |
| C、X3Y2 |
| D、X2Y |
下列微粒中与Na+具有相同的质子数和电子数的微粒是( )
| A、H2O |
| B、H3O+ |
| C、OH- |
| D、NH3 |
从原子序数11依次增加到17,下列所叙递变关系错误的是( )
| A、最外层电子数逐渐增多 |
| B、原子半径逐渐增大 |
| C、最高正价数值逐渐增大 |
| D、从硅到氯负价从-4-1 |
有关NA说法正确的是( )
| A、22.4L的SO3中含有NA个硫原子 |
| B、常温常压下,18g的水含有的电子数为NA |
| C、500mL 1mol/L Fe2(SO4)3溶液,通250mL 3mol/L 的Na2SO4溶液所含硫酸根离子的物质的量浓度之比为1:1 |
| D、足量的Fe与1mol氯气充分反应,则转移电子数为2NA |
下列说法正确的是( )
| A、在周期表中金属和非金属的分界处寻找催化剂和耐高温、耐腐蚀的合金材料 |
| B、元素性质随着核电荷数的递增而呈周期性的变化叫元素周期律 |
| C、绿色植物进行光合作用时,将太阳能转化为化学能“贮存”起来 |
| D、相对分子质量相同,而结构不同的化合物互称为同分异构体 |
下列说法正确的是( )
| A、联合制碱法的优点是减少了对设备的腐蚀 |
| B、工业生产硫酸时,用98%硫酸的来吸收三氧化硫,可以避免形成酸雾并提高吸收率 |
| C、合成氨是天然固氮的方法之一 |
| D、碳酸钠俗称小苏打,甲烷是一种清洁能源 |