题目内容
14. 国产航母001A等舰艇的船底都涂有含Cu2O的防污涂料,制备Cu2O的一种方法为:
国产航母001A等舰艇的船底都涂有含Cu2O的防污涂料,制备Cu2O的一种方法为:Zn+2CuSO4+2NaOH=Cu2O+ZnSO4+Na2SO4+H2O.该反应的下列说法正确的是( )
| A. | Zn得到电子 | B. | CuSO4被氧化 | C. | NaOH是还原剂 | D. | CuSO4是氧化剂 |
分析 由反应可知:Zn+2CuSO4+2NaOH=Cu2O+ZnSO4+Na2SO4+H2O,锌失电子,发生氧化反应,铜离子得电子生成亚铜,发生还原反应,由此分析解答.
解答 解:由反应可知:Zn+2CuSO4+2NaOH=Cu2O+ZnSO4+Na2SO4+H2O,锌失电子,发生氧化反应,铜离子得电子生成亚铜,发生还原反应,
A、Zn由0价变成+2价,失电子,故A错误;
B、CuSO4被还原,而不是被氧化,故B错误;
C、NaOH中各元素化合价未变,既不是氧化剂,也不是还原剂,故C错误;
D、硫酸铜中铜元素的化合价降低是氧化剂,故D正确;
故选D.
点评 本题考查氧化还原反应中基本概念,学生从元素化合价入手分析解答,比较容易.

练习册系列答案
相关题目
4.下列各组物质熔点高低的比较,正确的是( )
| A. | 晶体硅>金刚石>碳化硅 | B. | CsCl>KCl>NaCl | ||
| C. | SiO2>CO2>He | D. | Br2>I2>He |
5.实验室可以用来直接加热的玻璃仪器是( )
| A. | 小试管 | B. | 容量瓶 | C. | 量筒 | D. | 蒸发皿 |
2.《中国能源矿产地质调查报告》显示我国天然气水合物超千亿吨油当量.天然气主要成分为( )
| A. | H2 | B. | CO | C. | CH4 | D. | C2H4 |
9.既可用排水法又可用向上排空气法收集的气体是( )
| A. | NO | B. | O2 | C. | NH3 | D. | NO2 |
19.用蘸有浓氨水的棉棒检漏输氯管道的原理为:3Cl2+8NH3═N2+6NH4Cl.该反应的下列说法正确的是( )
| A. | 35.5g氯气所含的分子数为6.02×1023 | |
| B. | 常温常压下,22.4L氨气所含原子总数为4×6.02×1023 | |
| C. | 反应每生成1molN2转移电子数约为6×6.02×1023 | |
| D. | 1mol•L-1NH4Cl溶液中,含有Cl-数约为6.02×1023 |
6.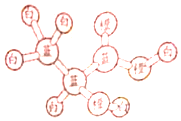 某有机物分子的球棍模型如图所示,图中“棍”代表化学键,不同颜色的“球”代表不同元素的原子,下列说法错误的是( )
某有机物分子的球棍模型如图所示,图中“棍”代表化学键,不同颜色的“球”代表不同元素的原子,下列说法错误的是( )
 某有机物分子的球棍模型如图所示,图中“棍”代表化学键,不同颜色的“球”代表不同元素的原子,下列说法错误的是( )
某有机物分子的球棍模型如图所示,图中“棍”代表化学键,不同颜色的“球”代表不同元素的原子,下列说法错误的是( )| A. | 1mol该有机物可与2molNa反应,生成1mol气体 | |
| B. | 该有机物可以发生加聚反应 | |
| C. | 该有机物可以发生取代反应,氧化反应、酯化反应 | |
| D. | 该有机物可以生成分子式为C6H8O4的酯 |
3.下列根据实验操作和现象所得出的结论错误的是( )
| A. | 用酒精灯外焰加热铝箔,铝箔熔化但不滴落,说明Al2O3>Al | |
| B. | 锅炉水垢CaSO4可用Na2CO3溶液浸泡,再用酸溶解去除,说明Ksp:CaCO3>CaSO4 | |
| C. | 向Na2SiO3溶液中通入适量CO2气体,有白色沉淀生成,说明酸性:H2CO3>H2SiO3 | |
| D. | 当光束通过淀粉溶液时,出现一条光亮的“通路”,说明分散质微粒的直径在1-100nm之间 |
10.从海水提取溴的过程中,有如下反应:5NaBr+NaBrO3+3H2SO4═3Br2+3Na2SO4+3H2O,与上述反应在原理上最相似的反应是( )
| A. | 2NaBr+Cl2═Br2+2NaCl | |
| B. | AlCl3+3NaAlO2+6H2O═4Al(OH)3↓+3NaCl | |
| C. | 2H2S+SO2═3S↓+2H2O | |
| D. | Cl2+H2O═HCl+HClO |