题目内容
将0.2molMnO2和50mLl2mol·L-1盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为( )(不考虑盐酸的挥发)
A.等于0.3 mol
B.小于0.3mol
C.大于0.3mol、小于0.6mol
D.以上结论都不正确
C
【解析】
试题分析:MnO2与浓盐酸反应制取Cl2的化学方程式为:MnO2+4HCl(浓)△MnCl2+Cl2↑+2H2O,n(HCl)=0.05 L×12 mol·L-1=0.6 mol,若只从方程式上看,0.6 mol HCl的能产生0.15 mol Cl2,但随着反应的进行,浓盐酸变成稀盐酸后MnO2与稀盐酸不反应,故放出的Cl2小于0.15 mol,溶液中Cl-的物质的量大于0.3mol、小于0.6mol,生成AgCl沉淀物质的量大于0.3mol、小于0.6mol,选C。
考点:考查根据化学方程式计算、氯气的实验室制备。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
已知:N2(g)+3H2(g) 2NH3(l) △H= -132 kJ/mol,蒸发1mol NH3(l)需要吸收的能量为20kJ,相关数据如下
2NH3(l) △H= -132 kJ/mol,蒸发1mol NH3(l)需要吸收的能量为20kJ,相关数据如下
| H2(g) | N2(g) | NH3(g) |
1mol分子中的化学键形成时要释放出的能量/kJ | 436 | 946 | a |
一定条件下,在体积1L的密闭容器中加入1molN2(g)和3molH2(g)充分反应,生成NH3(g)放出热量QkJ,
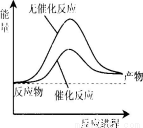
下列说法正确的是
A.上图可表示合成氨过程中的能量变化
B.a的数值为1173
C.Q的数值为92
D.其它条件相同,反应使用催化剂时释放出的能量大于无催化剂时释放出的能量