题目内容
20.设NA表示阿伏加德罗常数的值,下列说法正确的是( )| A. | 一定温度下,pH=6的纯水中含有OH-的数目为10-6NA | |
| B. | 120 g NaHSO4固体中含有的离子总数为2NA | |
| C. | 标准状况下,22.4 L己烷中所含分子的数目为NA | |
| D. | 100 mL 0.5 mol•L-1的(NH4)2SO4溶液中,NH4+的数目为0.1NA |
分析 A.一定温度离子积常为10-12,计算氢氧根离子浓度为10-6mol/L,溶液体积不知不能计算微粒数;
B.硫酸氢钠固体是钠离子和硫酸氢根离子构成;
C.标况下22.4L己烷不是气体
D.氨根离子为弱碱阳离子,部分发生水解.
解答 解:A.一定温度下,pH=6的纯水中,离子积常为10-12,氢氧根离子浓度为10-6mol/L,溶液体积不知不能计算氢氧根微粒数,故A错误;
B.120g NaHSO4固体的物质的量为$\frac{120g}{120g/mol}$=1mol,含有的离子总数为2NA,故B正确;
C.标准状况下己烷不是气体,22.4L己烷的物质的量不是1mol,故C错误;
D.氨根离子为弱碱阳离子,部分发生水解,所以100mL 0.5mol/L-1的(NH4)2SO4溶液中,NH4+的数目小于0.1NA,故D错误;
故选:B.
点评 本题考查了阿伏伽德罗常数的应用,掌握阿伏伽德罗常数与物质的量、摩尔质量等物理量之间的转化关系,注意盐类的水解规律,题目难度不大.

练习册系列答案
相关题目
10.新型无机材料碳化钛(TiC)、碳化硼(B4C)、氮化硅(Si3N4)等称为非氧化物陶瓷,合成这些物质需在高温下进行,在合成工艺中必须注意( )
| A. | 通入充足的氧气 | B. | 避免与氧气接触 | ||
| C. | 可在氮气气氛中合成 | D. | 通入少量氧气 |
11.下列说法正确的是(NA表示阿伏加德罗常数的数值)( )
| A. | 在常温常压下,11.2 L N2含有的分子数为0.5 NA | |
| B. | 2.4g Mg变为Mg2+时失去的电子数目为0.2NA | |
| C. | 1 L 1mol•L-1 CH3COONa溶液中存在NA个CH3COO- | |
| D. | 1 mol Cn H2n+2含有(3n+2)NA个共价键 |
8.分枝酸可用于生化研究,其结构简式如图.下列关于分枝酸的叙述正确的是( )
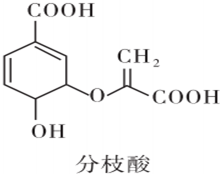

| A. | 其分子式为C10H8O6 | |
| B. | 可与乙醇、乙酸反应,且反应类型相同 | |
| C. | 1 mol分枝酸在一定条件下最多可与3 mol NaOH发生反应 | |
| D. | 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同 |
15.下列物质的主要成分不是SiO2的是( )
| A. | 石英 | B. | 水晶 | C. | 金刚砂 | D. | 玛瑙 |
5.下列离子方程式书写正确的是( )
| A. | 铜和稀硝酸反应 Cu+4H++NO3-=Cu2++2H2O+NO↑ | |
| B. | 碳酸氢钠的水解 HCO3-+H2O=H2CO3+OH- | |
| C. | Fe投入盐酸中 2Fe+6H+=2Fe3++3H2↑ | |
| D. | 氢氧化铝溶于氢氧化钠溶液 Al(OH)3+OH-=AlO2-+2H2O |
12.下列物质前者是强电解质、后者是弱电解质的是( )
| A. | KNO3 CH3COOH | B. | HCl NaHSO4 | C. | NaCl BaSO4 | D. | NH3•H2O H2SO4 |
9.下列叙述正确的是( )
| A. | 1mol Cl2中约含有6.02×1023个氯原子 | |
| B. | 1mol OH-的质量为17g | |
| C. | 1mol O2的体积约为22.4L | |
| D. | 1mol氢中含有2mol 电子 |
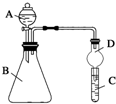 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.