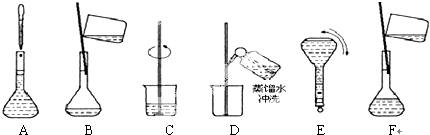
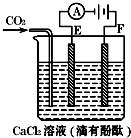
题目内容
室温下,Ksp[Mg(OH)2]远大于Ksp[Al(OH)3].向浓度均为0.1mol/L的MgCl2和AlCl3混合溶液中,逐滴加入NaOH溶液.下列示意图表示生成沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系,合理的是( )
A、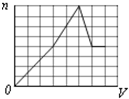 |
B、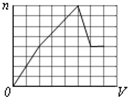 |
C、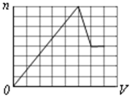 |
D、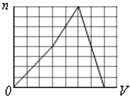 |
考点:镁、铝的重要化合物
专题:图示题
分析:浓度均为0.1mol?L-1的MgCl2和AlCl3混合溶液中,溶液中镁离子、铝离子的浓度相同为0.1mol/L,Mg(OH)2的Ksp或溶解度远大于Al(OH)3,故向混合溶液逐滴加入NaOH溶液,铝离子首先转化为氢氧化铝沉淀,当铝离子完全沉淀,镁离子再转化为氢氧化镁沉淀,当镁离子沉淀完全,再加入氢氧化钠,氢氧化铝溶解,沉淀的质量减少,由于氢氧化镁不溶于碱,故沉淀减少到一定值不再变化,为氢氧化镁的物质的量.据此结合图象分析.
解答:
解:浓度均为0.1mol?L-1的MgCl2和AlCl3混合溶液中,溶液中镁离子、铝离子的浓度相同为0.1mol/L,Mg(OH)2的Ksp或溶解度远大于Al(OH)3,故向混合溶液逐滴加入NaOH溶液,铝离子首先转化为氢氧化铝沉淀,当铝离子完全沉淀,镁离子再转化为氢氧化镁沉淀,当镁离子沉淀完全,再加入氢氧化钠,氢氧化铝溶解,沉淀的质量减少,Al(OH)3+OH-═AlO2-+2H2O,在图中消耗一格氢氧化钠体积,那么开始要铝离子完全沉淀,Al3++3OH-=Al(OH)3↓,在图中消耗三格氢氧化钠体积,由于氢氧化镁不溶于碱,故沉淀减少到一定值不再变化,为氢氧化镁的物质的量.
故选A.
故选A.
点评:本题考查铝及化合物的性质、化学反应图象等,根据反应过程判断沉淀与氢氧化钠体积关系,注意纵坐标表示沉淀的物质的量,不是氢氧化铝.

练习册系列答案
相关题目
下列鉴别方法不可行的是( )
| A、用水鉴别1-丙醇、甲苯和硝基苯 |
| B、用燃烧法鉴别甲醇、苯和四氯化碳 |
| C、用饱和碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯 |
| D、用溴水鉴别乙苯、苯酚、环己烷和乙醇 |
现有不纯的氯化铜粉末13.5g(内含一种杂质).当与足量的AgNO3溶液反应时,生成29gAgCl沉淀,则粉末中的杂质可能是( )
| A、FeCl3 |
| B、KCl |
| C、ZnCl2 |
| D、BaCl2 |
石油气中主要成份是烷烃.某石油气充分燃烧后,在相同条件下测得生成的二氧化碳的体积是该石油气体积的1.5倍,则石油气中一定有( )
| A、甲烷 | B、乙烷 | C、丁烷 | D、戊烷 |
化学在人类生活中扮演着重要角色,以下应用不正确的是( )
| A、使用无磷洗衣粉,可彻底解决水体富营养化问题 |
| B、应用高效洁净的能源转换技术有利于节能减排、保护环境 |
| C、用浸泡过高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可达到水果保鲜的目的 |
| D、合理开发利用可燃冰(固态甲烷水合物)有助于缓解能源紧缺 |
电解熔融的氧化铝,当电路中通过10mol电子时,理论上析出铝的质量是( )
| A、90g | B、180g |
| C、270g | D、360g |