题目内容
13.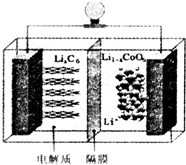 随着各地“限牌”政策的推出,电动汽车成为汽车族的“新宠”.某电动汽车使用的是钴酸锂(LiCoO2)电池,其工作原理如图所示,且电解质为一种能传导Li+的高分子材料,隔膜只允许Li+通过,电池反应式为LixC6+Li1-xCoO2$?_{充电}^{放电}$C6+LiCoO2.下列说法不正确的是( )
随着各地“限牌”政策的推出,电动汽车成为汽车族的“新宠”.某电动汽车使用的是钴酸锂(LiCoO2)电池,其工作原理如图所示,且电解质为一种能传导Li+的高分子材料,隔膜只允许Li+通过,电池反应式为LixC6+Li1-xCoO2$?_{充电}^{放电}$C6+LiCoO2.下列说法不正确的是( )| A. | 放电时,正极锂的化合价未发生改变 | |
| B. | 充电时Li+移动方向:右室→左室 | |
| C. | 放电时负极的电极反应式:LixC6-xe-═C6+xLi+ | |
| D. | 充电时阳极的电极反应式:Li1-xCoO2+xLi++xe-═LiCoO2 |
分析 根据电池反应式知,负极反应式为LixC6-xe-=C6+xLi+、正极反应式为Li1-xCoO2+xLi++xe-=LiCoO2,充电时,阴极、阳极反应式与负极、正极反应式正好相反,所以A是负极、B是正极,根据二次电池的工作原理结合原电池和电解池的工作原理来回答.
解答 解:根据电池反应式知,负极反应式为LixC6-xe-=C6+xLi+、正极反应式为Li1-xCoO2+xLi++xe-=LiCoO2,充电时,阴极、阳极反应式与负极、正极反应式正好相反,所以左端是负极、右端是正极,
A、放电时,正极反应式为Li1-xCoO2+xLi++xe-=LiCoO2,正极锂的化合价未发生改变,故A正确;
B、充电时,A是阴极、B是阳极,锂离子向阴极移动,则Li+从右边流向左边,故B正确;
C、放电时,A是负极,发生失电子的氧化反应,电极反应式为:LixC6-xe-=C6+xLi+,故C正确;
D、充电时,B电极是阳极,发生失电子的氧化反应,电极反应式为LiCoO2-xe-=Li1-xCoO2+xLi+,故D错误;
故选D.
点评 本题考查化学电源新型电池,侧重考查原电池和电解池原理,明确充放电各个电极上发生的反应是解本题关键,难点是电极反应式的书写,题目难度不大.

练习册系列答案
相关题目
1.下列化学用语表示正确的是( )
| A. | N2的电子式: | |
| B. | 乙酸的结构简式:C2H4O2 | |
| C. | S2-的结构示意图: | |
| D. | 氢氧化钡的电离方程式:Ba(OH)2═Ba2+(OH)${\;}_{2}^{2-}$ |
18.研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义.CO可用于炼铁,已知:
Fe2O3(s)+3C(s)═2Fe(s)+3CO(g)△H1=+489.0kJ•mol-1
C(s)+CO2(g)═2CO(g)△H2=+172.5kJ•mol-1;则CO还原Fe2O3(s)的热化学方程式为( )
Fe2O3(s)+3C(s)═2Fe(s)+3CO(g)△H1=+489.0kJ•mol-1
C(s)+CO2(g)═2CO(g)△H2=+172.5kJ•mol-1;则CO还原Fe2O3(s)的热化学方程式为( )
| A. | Fe2O3+3CO=═2Fe+3CO2△H=-28.5 kJ•mol-1 | |
| B. | Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-28.5 kJ | |
| C. | Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=+28.5 kJ•mol-1 | |
| D. | Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-28.5 kJ•mol-1 |
2.NA代表阿伏加德罗常数的值,下列有关说法正确的是( )
| A. | 1 mol 羟基(-OH)含有的电子数为10 NA | |
| B. | 高温下,0.2 mol Fe与足量水蒸气反应,生成H2的分子数为0.3 NA | |
| C. | 7.8 g Na2S、Na2O2的固体混合物中含有的阴离子数为0.1 NA | |
| D. | 用惰性电极电解饱和食盐水,电路中通过NA个电子,则阳极产生气体11.2 L |
3.下列反应的离子方程式书写正确的是( )
| A. | 硫酸铜溶液与氢氧化钡溶液混合:Ba2++SO42-═BaSO4↓ | |
| B. | 大理石投入稀硝酸中:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 氨水与硫酸铝溶液混合:Al3++4NH3?H2O═AlO2-+4NH4++2H2O | |
| D. | 氯水通入水中:Cl2+H2O═Cl-+ClO-+2H+ |
 .
.


