题目内容
12.某同学设计下列实验,来研究硫酸和硝酸的性质.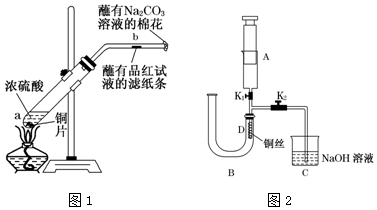
实验一:在一支试管中放入一块很小的铜片,再加入2mL浓硫酸,然后把试管固定在铁架台上.把一小条蘸有品红溶液的滤纸放入带有单孔橡皮塞的玻璃管中.塞紧试管口,在玻璃管口处缠放一团蘸有Na2CO3溶液的棉花.给试管加热,观察现象.当试管中的液体逐渐透明时,停止加热.待试管中的液体冷却后,将试管中的液体慢慢倒入另一支盛有少量水的试管中,观察现象.
回答下列问题:
(1)a处反应的化学方程式为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,计算放出112mL气体(标准状况),转移电子的物质的量为0.01mol.
(2)试管中的液体反应一段时间后,b处滤纸条的变化为蘸有品红溶液的滤纸条褪色.
待试管中反应停止后,给玻璃管放有蘸过品红溶液的滤纸处微微加热,滤纸条的变化为滤纸变红.
实验二:为了证明铜与稀硝酸反应产生一氧化氮,某同学设计了一个实验,其装置如图2所示(加热装置和固定装置均已略去).A为注射器,B为两端长短不等的U形管,C是装有NaOH溶液的烧杯,D处是绕成螺旋状的铜丝,K1、K2是止水夹.
(1)实验时,为在D处收集到NO,以便观察颜色,必须事先在A中吸入一定量的空气.然后关闭K1(“关闭”或“打开”),从U形管左端注入稀硝酸.
(2)然后给装置B微微加热,在装置D处产生无色气体,其反应的离子方程式为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O.
(3)如何证明D处聚集的是NO而不是H2?打开止水夹K1,把注射器中的空气压入U形管中,若观察到D处气体变红棕色,则证明收集的是NO,而不是H2.
(4)实验现象观察完毕,关闭止水夹K1,打开止水夹K2,在重力作用下,U形管右端的红棕色混合气体被酸液压入NaOH溶液中吸收,消除了环境污染.
分析 实验一:(1)铜和浓硫酸在加热条件下能发生反应,生成硫酸铜和二氧化硫、水;结合反应方程式计算出转移的电子的物质的量;
(2)二氧化硫能使品红溶液褪色,但二氧化硫的漂白性不稳定,加热时会恢复原来的颜色;
实验二:(1)在A中吸入一定量的空气,然后关闭K1,打开止水夹 K2,使铜与稀硝酸反应生成的一氧化氮进入集气瓶;若U形管右端稀硝酸接触胶塞时,U形管中空气已被排净;
(2)稀硝酸与铜反应生成硝酸铜和NO和水,据此写出反应的离子方程式;
(3)NO为无色,用到空气后一氧化氮与氧气反应生成红棕色的二氧化氮,据此可检验NO.
解答 解:实验一:(1)浓硫酸具有强氧化性,能和铜反应,被铜还原为二氧化硫,所以产物有生成的硫酸铜、二氧化硫和水;书写化学方程式为:Cu+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
标况下112mL二氧化硫的物质的量为:$\frac{0.112L}{22.4L/mol}$=0.005mol,生成0.005mol二氧化硫转移的电子为:0.005mol×(6-4)=0.01mol;
故答案为:Cu+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;0.01 mol;
(2)二氧化硫能和有色物质生成无色物质,二氧化硫能使品红溶液褪色,所以二氧化硫具有漂白性;但生成的无色物质不稳定,加热时会恢复原来的颜色;
故答案为:蘸有品红溶液的滤纸条褪色;滤纸变红;
实验二:(1)在A中吸入一定量的空气,然后关闭K1,打开止水夹K2,使铜与稀硝酸反应生成的一氧化氮进入集气瓶,当U形管右端稀硝酸接触胶塞时,可以确定U形管中空气已被赶尽,
故答案为:关闭;
(2)稀硝酸与铜反应生成硝酸铜和NO,反应的离子方程式为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,
故答案为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O;
(3)B中硝酸和铜反应生成NO,易与氧气反应,则将A中空气压入B中,会有红棕色气体生成,如果观察到红棕色,则说明生成NO而不是氢气,
故答案为:打开止水夹K1,把注射器中的空气压入U形管中,若观察到D处气体变红棕色,则证明收集的是NO,而不是H2.
点评 本题考查了性质实验方案的设计,题目难度中等,熟练掌握浓硫酸、浓硝酸的化学性质为解答关键,明确性质实验方案的设计与评价原则,试题涉及知识点较多、综合性较强,充分考查学生的分析、理解能力及化学实验能力.

 阅读快车系列答案
阅读快车系列答案| A. | 一定不存在Ba2+,NH4+可能存在 | B. | CO32-一定存在 | ||
| C. | Na+一定存在 | D. | 一定不存在Cl- |
 氢气是新型能源和重要化工原料.
氢气是新型能源和重要化工原料.已知:①2CO(g)+O2(g)=2CO2(g)△H1
②CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H2
③H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H2
(1)科学家提出一种利用天然气制备氢气的方法:CH4(g)+CO2(g)=2CO(g)+2H2(g)△H,△H=△H2-△H1-2△H3,这种方法的推广与使用,不仅实现资源综合利用,而且还能解决环境问题是减少二氧化碳排放,缓解温室效应.
(2)氨气是重要化工原料,在国民经济中占重要地位.
①在恒温、容积相等的恒容密闭容器中投入一定量氮气、氢气,发生如下可逆反应:
N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ•mol-1
实验测得起始、平衡时的有关数据如表所示:
| 容器编号 | 起始时各物质的物质的量/mol | 平衡时反应中的能量变化 | ||
| H2 | N2 | NH3 | ||
| Ⅰ | 3n | n | 0 | 放出热量a kJ |
| Ⅱ | 3n | 2n | 0 | 放出热量b kJ |
| Ⅲ | 6n | 2n | 0 | 放出热量c kJ |
A.N2的转化率:Ⅱ>I>Ⅲ
B.放出热量:a<b<92.4n
C.达到平衡时氨气的体积分数:Ⅲ>Ⅰ
D.平衡常数:Ⅲ>Ⅱ>Ⅰ
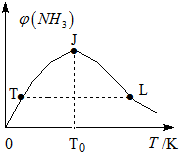
②在密闭恒容容器中投入一定量氮气和氢气,混合气体中氨气体积分数和温度关系如图所示:
曲线TJ段变化主要原因是平衡之前,反应向生成氨方向进行,JL段变化的主要原因是该正反应是放热反应,平衡之后,升高温度,平衡向逆方向移动,促进氨分解,氨的体积分数减小,氨气正反应速率:T点小于小于L点(填:大于、小于或等于).
③在2L密闭容器中充入一定量的氨气,氨气的物质的量与反应时间关系如表所示:
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | … |
| NH3/mol | 2 | 1.0 | 0.5 | 0.25 | 0.24 | 0.24 |
④常温下,在V mL的a mol•L-1稀硫酸溶液中滴加b mol•L-1稀氨水V mL恰好使混合溶液呈中性.此时,一水合氨的电离常数Kb=$\frac{2a}{(b-2a)×1{0}^{7}}$(用含a、b代数式表示).
(3)氢气直接作燃料电池的理论输出电压为1.2V,能量密度E=$\frac{\frac{1.2V×\frac{1000g}{2g/mol×2×96500C/mol}}{1kg}}{3.6×1{0}^{6}J•k{W}^{-1}•{h}^{-1}}$=32.2kW•h•kg-1(列式计算,精确到小数点后一位.提示:能量密度=电池输出电能/燃料质量,1kW•h=3.6×106J,常用单位为kW•h•kg-1).
| A. | 纯净水 | B. | 0.lmol/LHCl | C. | 1.0mol/LCH3COOH | D. | 0.5mol/LH2SO4 |
| A. | C+H2O $\frac{\underline{\;高温\;}}{\;}$CO+H2 | B. | 3NO2+H2O=2HNO3+NO | ||
| C. | Cl2+SO2+H2O=H2SO4+2HCl | D. | 2F2+2H2O=4HF+O2 |
| A. | x=0.6a 2Fe2++Cl2=2Fe3++2Cl- | |
| B. | x=a 2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl- | |
| C. | x=0.4a 2Br-+Cl2=Br2+2Cl- | |
| D. | x=2a 2Fe2++6Br-+4Cl2=3Br2+2Fe3++8Cl- |