题目内容
下图是一个化学过程的示意图.已知甲池的总反应式为:
2CH3OH+3O2+4KOH═2K2CO3+6H2O 填写下列空白:
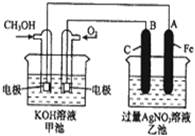
(1)请写出甲、乙两池的名称.甲池是 ,乙池是 .
(2)甲池中通入O2的电极名称是 ,电极反应方程式为 ;乙池中A(Fe)电极的电极反应式是 .
(3)反应过程中,甲池溶液pH的变化为(升高、降低或不变 ) .
(4)当乙池中A(Fe)极的质量增加5.40g时,甲池中理论上消耗O2 mL(标准状况下)
2CH3OH+3O2+4KOH═2K2CO3+6H2O 填写下列空白:

(1)请写出甲、乙两池的名称.甲池是
(2)甲池中通入O2的电极名称是
(3)反应过程中,甲池溶液pH的变化为(升高、降低或不变 )
(4)当乙池中A(Fe)极的质量增加5.40g时,甲池中理论上消耗O2
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)甲池能自发的进行氧化还原反应而构成原电池,则乙池为电解池;
(2)甲池中通入燃料的电极是负极、通入氧化剂的电极是正极,正极上氧气得电子和水反应生成氢氧根离子,乙池中A是阴极,阴极上银离子得电子发生还原反应;
(3)甲中电池反应式为2CH3OH+3O2+4KOH═2K2CO3+6H2O,放电过程中,氢氧根离子浓度降低;
(4)串联电路中转移电子相等.
(2)甲池中通入燃料的电极是负极、通入氧化剂的电极是正极,正极上氧气得电子和水反应生成氢氧根离子,乙池中A是阴极,阴极上银离子得电子发生还原反应;
(3)甲中电池反应式为2CH3OH+3O2+4KOH═2K2CO3+6H2O,放电过程中,氢氧根离子浓度降低;
(4)串联电路中转移电子相等.
解答:
解:(1)甲池能自发的进行氧化还原反应而构成原电池,乙池有外接电源,所以乙池为电解池,
故答案为:原电池;电解池;
(2)甲池中通入燃料的电极是负极、通入氧化剂的电极是正极,所以通入氧气的电极是正极,正极上氧气得电子和水反应生成氢氧根离子,电极反应式为O2+4e-+2H2O=4OH-;乙池中A是阴极,阴极上银离子得电子发生还原反应,电极反应式为Ag++e-=Ag,
故答案为:正极;O2+4e-+2H2O=4OH-;Ag++e-=Ag;
(3)甲中电池反应式为2CH3OH+3O2+4KOH═2K2CO3+6H2O,放电过程中,氢氧根离子参加反应而导致浓度降低,所以溶液的pH降低,
故答案为:降低;
(4)铁电极上析出银,A(Fe)极的质量增加5.40g时转移电子的物质的量=
×1=0.05mol,根据串联电路中转移电子相等,得甲池中理论上消耗O2体积=
×22.4L/mol=280mL,
故答案为:280.
故答案为:原电池;电解池;
(2)甲池中通入燃料的电极是负极、通入氧化剂的电极是正极,所以通入氧气的电极是正极,正极上氧气得电子和水反应生成氢氧根离子,电极反应式为O2+4e-+2H2O=4OH-;乙池中A是阴极,阴极上银离子得电子发生还原反应,电极反应式为Ag++e-=Ag,
故答案为:正极;O2+4e-+2H2O=4OH-;Ag++e-=Ag;
(3)甲中电池反应式为2CH3OH+3O2+4KOH═2K2CO3+6H2O,放电过程中,氢氧根离子参加反应而导致浓度降低,所以溶液的pH降低,
故答案为:降低;
(4)铁电极上析出银,A(Fe)极的质量增加5.40g时转移电子的物质的量=
| 5.40g |
| 108g/mol |
| 0.05mol |
| 4 |
故答案为:280.
点评:本题考查了原电池和电解池原理,根据得失电子确定正负极、阴阳极,再结合各个电极上发生的反应来分析解答,注意守恒思想的运用,题目难度不大.

练习册系列答案
相关题目
下列反应的离子方程式正确的是( )
A、实验室用NH4Cl和Ca(OH)2固体混合加热制NH3:NH
| ||||||
B、NaOH与NH4Cl溶液混合加热:NH
| ||||||
C、氨水加入盐酸中:NH3?H2O+H+═NH
| ||||||
| D、氨气通入稀H2SO4中:NH3+H+═NH4+ |
在下列条件的溶液中,各组离子一定能够大量共存的是( )
| A、使酚酞试液变红的溶液:Na+、Cl-、SO42-、Fe3+ |
| B、无色透明溶液中:K+、SO42-、MnO4-、H+ |
| C、可与锌反应放出氢气的溶液中:Na+、Ca2+、Cl-、HCO3- |
| D、使pH试纸变蓝的溶液中:Ba2+、Na+、NO3-、Cl- |

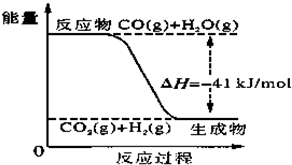 已知工业制氢气的反应为CO(g)+H2O(g)?CO2(g)+H2(g),反应过程中能量变化如图所示.在500℃时的平衡常数K=9.若在2L的密闭容器中CO和水蒸气的起始浓度都是0.1mol/L,10min时达到平衡状态.
已知工业制氢气的反应为CO(g)+H2O(g)?CO2(g)+H2(g),反应过程中能量变化如图所示.在500℃时的平衡常数K=9.若在2L的密闭容器中CO和水蒸气的起始浓度都是0.1mol/L,10min时达到平衡状态.