题目内容
13.不属于NO3-的等电子体的是( )| A. | NO2 | B. | BF3 | C. | SO3 | D. | NF32+ |
分析 根据等电子体是指具有相同价电子总数和原子总数的分子或离子来回答.
解答 解:NO3-中有4个原子,5+6×3+1=24个价电子,
A.NO2中有3个原子,5+6×2=17个价电子,与NO3-不是等电子体,故A选;
B.BF3中有4个原子,3+7×3=24个价电子,与NO3-是等电子体,故B不选;
C.SO3中有4个原子,6+6×3=24个价电子,与NO3-是等电子体,故C不选;
D.NF32+中有4个原子,5+7×3-2=24个价电子,与NO3-是等电子体,故D不选.
故选:A.
点评 本题考查了等电子体的含义,解答本题的关键是要充分理解等电子体的本质特征,只有这样才能对问题做出正确的判断.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
15. NaCl和NaClO在酸性条件下可发生反应:ClO-+Cl-+2H+═Cl2↑+H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况.
NaCl和NaClO在酸性条件下可发生反应:ClO-+Cl-+2H+═Cl2↑+H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况.
(1)此消毒液中NaClO可吸收空气中的CO2生成NaHCO3和HClO而变质.写出化学反应方程式:NaClO+CO2+H2O=NaHCO3+HClO.
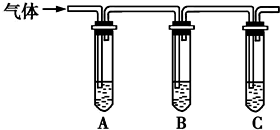
(2)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出.通过如图所示装置检验气体的成分,从而判断该消毒液是否变质.
限选试剂:98%浓硫酸、1%品红溶液、1.0mol•L-1 KI-淀粉溶液、1.0mol•L-1NaOH溶液、澄清石灰水、饱和NaCl溶液.
请完成下列实验方案(如图).
(3)用滴定法测定消毒液中NaClO的浓度.实验步骤如下:
①量取 25.00mL消毒液放入锥形瓶中,加入过量的a mol•L-1 Na2SO3溶液b mL.
②滴定分析.将c mol•L-1的酸性KMnO4溶液装入酸式(填“酸式”或“碱式”)滴定管中滴定,使KMnO4和剩余的Na2SO3发生反应.当溶液由无色变成浅红色,且半分钟内红色保持不褪去时,停止滴定,记录数据.重复滴定实验3次,测得平均消耗酸性KMnO4溶液V mL;滴定过程中涉及的反应有:NaClO+Na2SO3═NaCl+Na2SO4;2KMnO4+5Na2SO3+3H2SO4═K2SO4+2MnSO4+5Na2SO4+3H2O.
③计算.消毒液中NaClO的浓度为$\frac{2ab-5vc}{50}$mol•L-1(用含a、b、c、V的代数式表示).
 NaCl和NaClO在酸性条件下可发生反应:ClO-+Cl-+2H+═Cl2↑+H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况.
NaCl和NaClO在酸性条件下可发生反应:ClO-+Cl-+2H+═Cl2↑+H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况.(1)此消毒液中NaClO可吸收空气中的CO2生成NaHCO3和HClO而变质.写出化学反应方程式:NaClO+CO2+H2O=NaHCO3+HClO.
(2)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出.通过如图所示装置检验气体的成分,从而判断该消毒液是否变质.
限选试剂:98%浓硫酸、1%品红溶液、1.0mol•L-1 KI-淀粉溶液、1.0mol•L-1NaOH溶液、澄清石灰水、饱和NaCl溶液.
请完成下列实验方案(如图).
| 所加试剂 | 预期现象和结论 |
| 向试管A中加足量①1.0mol/LK淀粉溶液; 试管B中加1%品红溶液; 试管C中加②澄清石灰水. | 若A中溶液变蓝色,B中溶液不褪色,C中溶液变浑浊,则消毒液部分变质; ③若A中溶液变蓝色,B中溶液不退色(无变化),C中溶液不变浑浊(无变化),则消毒液未变质,则消毒液未变质; ④若A中溶液不变蓝色(无变化),B中溶液不退色(无变化),C中溶液变浑浊则消毒液完全变质,则消毒液完全变质. |
①量取 25.00mL消毒液放入锥形瓶中,加入过量的a mol•L-1 Na2SO3溶液b mL.
②滴定分析.将c mol•L-1的酸性KMnO4溶液装入酸式(填“酸式”或“碱式”)滴定管中滴定,使KMnO4和剩余的Na2SO3发生反应.当溶液由无色变成浅红色,且半分钟内红色保持不褪去时,停止滴定,记录数据.重复滴定实验3次,测得平均消耗酸性KMnO4溶液V mL;滴定过程中涉及的反应有:NaClO+Na2SO3═NaCl+Na2SO4;2KMnO4+5Na2SO3+3H2SO4═K2SO4+2MnSO4+5Na2SO4+3H2O.
③计算.消毒液中NaClO的浓度为$\frac{2ab-5vc}{50}$mol•L-1(用含a、b、c、V的代数式表示).
16.一种熔融碳酸盐燃料电池原理示意如图所示
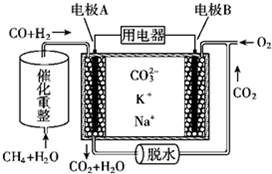
下列说法不正确的是( )

下列说法不正确的是( )
| A. | 电池工作时,K+向B极移动 | |
| B. | 电极B上发生的电极反应:O2+2CO2+4e-═2CO32- | |
| C. | 电池工作时,CO2可以循环利用 | |
| D. | 消耗1molCH4催化重整得到的CO和H2通入电极A,需要电极B同时通入33.6L的O2 |
1.A、B、C、D、E、F是中学化学中常见的六种短周期元素,有关位置及信息如下:A的气态氢化物水溶液呈碱性;C单质一般保存在煤油中;F的最高价氧化物对应的水化物既能与酸反应又能与碱反应,G单质是日常生活中用量最大的金属,易被腐蚀或损坏.请回答下列问题:
(1)A的最高价氧化物对应的水化物与其氢化物反应生成离子化合物的化学式为NH4NO3.
(2)由C、B、F三种元素构成的化合物中含有的化学键类型共价键和离子键
(3)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中其化学作用可能引发的后果有①③(填序号).
①酸雨 ②温室效应 ③光化学烟雾 ④臭氧层破坏
(4)若在D与G组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,可设计成的原电池,则其正极反应式为2Fe3++2e-=2Fe2+.
| … | E | A | B | ||
| C | … | D |
(2)由C、B、F三种元素构成的化合物中含有的化学键类型共价键和离子键
(3)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中其化学作用可能引发的后果有①③(填序号).
①酸雨 ②温室效应 ③光化学烟雾 ④臭氧层破坏
(4)若在D与G组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,可设计成的原电池,则其正极反应式为2Fe3++2e-=2Fe2+.
8.下列叙述正确的是( )
①锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率
②镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
③电镀时,应把待镀金属置于电解槽的阴极
④电解饱和氯化钠溶液可以冶炼出金属钠
⑤钢铁表面常易锈蚀生成Fe2O3•nH2O
⑥粗铜精炼时粗铜连接电源的正极
⑦金属的防护中,牺牲阳极的阴极保护法是让被保护金属做原电池的负极.
①锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率
②镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
③电镀时,应把待镀金属置于电解槽的阴极
④电解饱和氯化钠溶液可以冶炼出金属钠
⑤钢铁表面常易锈蚀生成Fe2O3•nH2O
⑥粗铜精炼时粗铜连接电源的正极
⑦金属的防护中,牺牲阳极的阴极保护法是让被保护金属做原电池的负极.
| A. | ①②③⑤⑥⑦ | B. | ①③⑤⑦ | C. | ①③⑤⑥ | D. | ①②③⑥⑦ |
18.设 NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 10mL20mol/L 浓硫酸与足量锌反应,转移电子数为 0.2NA | |
| B. | 0.1mol24Mg18O 晶体中所含中子总数为 2.0NA | |
| C. | 在标准状况下,2.8gN2和 2.24LCO 所含电子数均为 1.4NA | |
| D. | 1L1mol/L 的 NaClO 溶液中含有 ClO-的数目为 NA |
5.在日常生活中,下列解决问题的方法不可行的是( )
| A. | 为加快漂白精的漂白速率,使用时可滴加几滴醋酸 | |
| B. | 为避免船体遭受腐蚀,在船身上装铅块 | |
| C. | 为增强治疗缺铁性贫血效果,可在口服硫酸亚铁片时同服维生素C | |
| D. | 为使水果保鲜,可在水果箱内放入高锰酸钾溶液浸泡过的硅藻土 |
3.在由水电离产生的c(H+)=1×10-14mol•L-1的溶液中,一定可以大量共存的离子组是( )
| A. | K+、Na+、SO42-、CO32- | B. | NH4+、Al3+、Br-、SO42- | ||
| C. | Na+、Mg2+、Cl-、NO3- | D. | K+、Ba2+、Cl-、NO3- |