题目内容
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、22.4L O2中含有氧分子的个数为NA |
| B、24g Mg与足量氧气反应转移的电子数为2NA |
| C、28g N2中含有氮原子的个数为NA |
| D、1mol?L-1 MgCl2溶液中含有氯离子个数为2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.没有告诉在标准状况下,不能使用标况下的气体摩尔体积计算氧气的物质的量;
B.镁为2价金属,24g镁的物质的量为1mol,完全反应失去2mol电子;
C.28g氮气的物质的量为1mol,1mol氮气含有2mol氮原子;
D.没有告诉氯化镁溶液的体积,无法计算溶液中氯离子数目.
B.镁为2价金属,24g镁的物质的量为1mol,完全反应失去2mol电子;
C.28g氮气的物质的量为1mol,1mol氮气含有2mol氮原子;
D.没有告诉氯化镁溶液的体积,无法计算溶液中氯离子数目.
解答:
解:A.没有告诉在标况下,不能使用标况下的气体摩尔体积计算22.4L氧气的物质的量,故A错误;
B.24g、镁的物质的量为1mol,1mol镁完全反应失去2mol电子,反应转移的电子数为2NA,故B正确;
C.28g氮气的物质的量为1mol.1mol氮气中含有2mol氮原子,含有氮原子的个数为2NA,故C错误;
D.没有告诉1mol?L-1 MgCl2溶液的体积,无法计算溶液中氯离子的物质的量及数目,故D错误;
故选B.
B.24g、镁的物质的量为1mol,1mol镁完全反应失去2mol电子,反应转移的电子数为2NA,故B正确;
C.28g氮气的物质的量为1mol.1mol氮气中含有2mol氮原子,含有氮原子的个数为2NA,故C错误;
D.没有告诉1mol?L-1 MgCl2溶液的体积,无法计算溶液中氯离子的物质的量及数目,故D错误;
故选B.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件;掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系;选项D为易错点,注意分析题中数据是否齐全.

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A、常温常压下,48gO3和48gO2含有的氧原子数均为3NA |
| B、1.8g的NH4+离子中含有的电子数为0.1NA |
| C、11.2L氧气中所含有的原子数为NA |
| D、标准状况下,22.4 L水所含分子数为NA |
下列措施不符合“绿色化学”思想的是( )
| A、循环使用物料 |
| B、用水代替有机溶剂 |
| C、直接排放电镀废水 |
| D、发展原子利用率达到100%的化学反应 |
Se是人体必需的微量元素,其中
Se的原子棱内中子数是( )
80 34 |
| A、80 | B、46 | C、34 | D、12 |

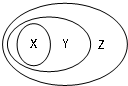 用如图表示的一些物质或概念间的从属关系中不正确的是( )
用如图表示的一些物质或概念间的从属关系中不正确的是( )