题目内容
往含0.2mol NaOH和0.1mol Ca(OH)2的溶液中持续稳定地通入CO2气体,当通入气体为6.72L(S.T.P)时立即停止,则这一过程中,溶液中离子的物质的量和通入CO2气体的体积关系正确的图象是(气体的溶解忽略不计)
- A.

- B.

- C.
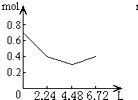
- D.

C
分析:n(CO2)= =0.3mol,通入含有0.2mol氢氧化钠和0.1mol氢氧化钙的溶液中,发生:
=0.3mol,通入含有0.2mol氢氧化钠和0.1mol氢氧化钙的溶液中,发生:
2OH-+CO2=CO32-+H2O,OH-+CO2=HCO3-+H2O,Ca2++CO32-=CaCO3↓,以此解答该题.
解答:n(CO2)= =0.3mol,
=0.3mol,
含有0.2mol氢氧化钠和0.1mol氢氧化钙的溶液中:n(OH-)=0.2mol+0.1mol×2=0.4mol,n(Na+)=0.2mol,
n(Ca2+)=0.1mol,
通入CO2,发生:2OH-+CO2=CO32-+H2O,OH-+CO2=HCO3-+H2O,Ca2++CO32-=CaCO3↓,
设生成xmolCO32-,ymolHCO3-,
则
x=0.1,y=0.2,
所以反应后溶液中含有:n(Na+)=0.2mol,n(HCO3-)=0.2mol,
可依次发生:①2OH-+CO2=CO32-+H2O,
②Ca2++CO32-=CaCO3↓,离子浓度迅速减小,
③OH-+CO2=HCO3-,
所以图象C符合,
故选C.
点评:本题考查离子方程式的计算,题目难度较大,解答本题时注意B和C的区别,为易错点.
分析:n(CO2)=
 =0.3mol,通入含有0.2mol氢氧化钠和0.1mol氢氧化钙的溶液中,发生:
=0.3mol,通入含有0.2mol氢氧化钠和0.1mol氢氧化钙的溶液中,发生:2OH-+CO2=CO32-+H2O,OH-+CO2=HCO3-+H2O,Ca2++CO32-=CaCO3↓,以此解答该题.
解答:n(CO2)=
 =0.3mol,
=0.3mol,含有0.2mol氢氧化钠和0.1mol氢氧化钙的溶液中:n(OH-)=0.2mol+0.1mol×2=0.4mol,n(Na+)=0.2mol,
n(Ca2+)=0.1mol,
通入CO2,发生:2OH-+CO2=CO32-+H2O,OH-+CO2=HCO3-+H2O,Ca2++CO32-=CaCO3↓,
设生成xmolCO32-,ymolHCO3-,
则
|
所以反应后溶液中含有:n(Na+)=0.2mol,n(HCO3-)=0.2mol,
可依次发生:①2OH-+CO2=CO32-+H2O,
②Ca2++CO32-=CaCO3↓,离子浓度迅速减小,
③OH-+CO2=HCO3-,
所以图象C符合,
故选C.
点评:本题考查离子方程式的计算,题目难度较大,解答本题时注意B和C的区别,为易错点.

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目



