题目内容
15.以溴乙烷为原料制取1,2-二溴乙烷,下列转化方案中最好的是( )| A. | CH3CH2Br$→_{△}^{HBr溶液}$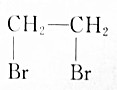 | |
| B. | CH3CH2Br$→_{光照}^{Br_{2}}$CH2BrCH2Br | |
| C. | CH3CH2Br$→_{△}^{NaOH醇溶液}$CH2═CH2$\stackrel{HBr}{→}$CH2BrCH3$→_{光照}^{Br_{2}}$CH2BrCH2Br | |
| D. | CH3CH2Br$→_{△}^{NaOH醇溶液}$CH2═CH2$\stackrel{溴水}{→}$CH2BrCH2Br |
分析 在有机物的制备反应中,应选择的合成路线是步骤尽量少,合成产率尽量高,据此解答即可.
解答 解:A、溴乙烷与溴化氢溶液不能反应,故A错误;
B、取代在有机物的制备反应中,取代位置不一,可能生成1,1-二溴乙烷,故B错误;
C、最后一步中,产物不唯一,故C错误;
D、先进行卤代烃的消去,引入双键,然后通过加成反应制备,可以制取纯净的1,2-二溴乙烷,故D正确,故选D.
点评 本题主要考查的是有机物的制备方案的设计,有机物的制备应尽量步骤少、产率高,难度不大.

练习册系列答案
相关题目
3.一定温度下的密度容器中发生:2HI(g)?I2(g)+H2(g),该反应达平衡状态的标志是( )
| A. | 气体的颜色不再发生变化 | |
| B. | 容器内的压强不再发生变化 | |
| C. | 单位时间内,每断裂2mol H-I键,同时有1mol I-I键生成 | |
| D. | 单位时间内,每断裂1mol H-H键,同时有1mol I-I键生成 |
20.A和B两元素能形成AB2型离子化合物,则A和B的原子序数可能是( )
| A. | 6和8 | B. | 11和8 | C. | 20和8 | D. | 20和17 |
20.按图示装置进行电解实验,随着实验进行下列数值变小的是( )


| A. | Cu2+物质的量浓度 | B. | Cl-物质的量浓度 | ||
| C. | Cu极质量 | D. | C(石墨)极质量 |
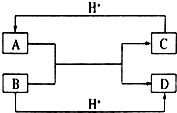 已知A、B、C、D是中学化学中常见的四种不同粒子,均是10电子的粒子,在通常情况下,C是气体,具有刺激性气味;D为液体.它们之间存在如图所示的转化关系(反应条件已经略去):
已知A、B、C、D是中学化学中常见的四种不同粒子,均是10电子的粒子,在通常情况下,C是气体,具有刺激性气味;D为液体.它们之间存在如图所示的转化关系(反应条件已经略去):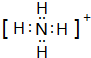 ;D
;D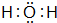 .写出B、C的离子符号或化学式:BOH-;CNH3.
.写出B、C的离子符号或化学式:BOH-;CNH3.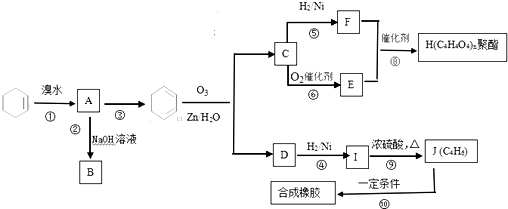
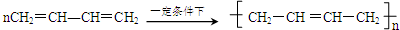 .
.