题目内容
8.Mg、Al混合物共0.4mol,用盐酸将其完全溶解,放出标准状况下11.2L气体,然后再滴入4mol/L 的NaOH溶液,请计算:(1)求该混合物中Mg、Al的物质的量
(2)若该Mg、Al的混合物与盐酸恰好完全反应,在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积为多少mL?
分析 (1)气体为氢气,n=$\frac{11.2L}{22.4L/mol}$=0.5mol,结合电子及原子守恒计算;
(2)该Mg、Al的混合物与盐酸恰好完全反应,在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,生成氢氧化镁、氢氧化铝,结合原子守恒计算.
解答 解:(1)体为氢气,n=$\frac{11.2L}{22.4L/mol}$=0.5mol,设Mg、Al的物质的量分别为x、y,则
$\left\{\begin{array}{l}{x+y=0.4}\\{2x+3y=0.5×2(1-0)}\end{array}\right.$
解得x=y=0.2mol,
答:该混合物中Mg、Al的物质的量均为0.2mol;
(2)该Mg、Al的混合物与盐酸恰好完全反应,在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,生成氢氧化镁、氢氧化铝,且不发生HCl与NaOH的反应,
由原子守恒可知,n(NaOH)=2n(Mg)+3n(Al)=2×0.2mol+3×0.2mol=1mol,需要NaOH溶液的体积为$\frac{1mol}{4mol/L}$=0.25L=250mL,
答:滴入NaOH溶液的体积为250mL.
点评 本题考查氧化还原反应的计算,为高频考点,把握电子及原子守恒为解答的关键,侧重分析与计算能力的考查,注意守恒法的应用,题目难度不大.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
18.下列实验操作中错误的是( )
| A. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 蒸馏中,冷却水应从冷凝管的下口通入,上口流出 | |
| D. | 过滤操作时,漏斗颈下端不能紧靠烧杯内壁 |
19.已知X2、Y2、Z2、W2四种物质的氧化能力依次减弱的顺序为W2、Z2、X2、Y2,下列氧化还原反应能发生的是( )
| A. | 2W-+Z2═2Z-+W2 | B. | 2X-+Z2═2Z-+X2 | C. | 2Y-+W2═2W-+Y2 | D. | 2Z-+X2═2X-+Z2 |
3.表是周期表中的一部分,根据A-I在周期表中的位置,用元素符号或化学式回答下列问题:
(1)表中元素,化学性质最不活泼的是Ne,只有负价而无正价的是F,氧化性最强的单质是F2.
(2)最高价氧化物的水化物碱性最强的是NaOH,酸性最强的是HClO4.
(3)A分别与G、H形成的化合物中,酸性强的是HCl.
(4)G、H的单质与水反应,更剧烈的是F2.
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(2)最高价氧化物的水化物碱性最强的是NaOH,酸性最强的是HClO4.
(3)A分别与G、H形成的化合物中,酸性强的是HCl.
(4)G、H的单质与水反应,更剧烈的是F2.
13.以锌锰废电池中的碳包为原料回收MnO2的过程中涉及如下反应:
①MnO2(s)+C(s)═MnO(s)+CO(g)△H1=+24.4kJ•mol-1
②MnO2(s)+CO(g)═MnO(s)+CO2(g)△H2=-148.1kJ•mol-1
③2MnO2(s)+C(s)═2MnO(s)+CO2(g)△H3
则下列判断正确的是( )
①MnO2(s)+C(s)═MnO(s)+CO(g)△H1=+24.4kJ•mol-1
②MnO2(s)+CO(g)═MnO(s)+CO2(g)△H2=-148.1kJ•mol-1
③2MnO2(s)+C(s)═2MnO(s)+CO2(g)△H3
则下列判断正确的是( )
| A. | 碱性锌锰干电池属于二次电池 | B. | △H3=△H1+△H2 | ||
| C. | 反应①的活化能为24.4 kJ•mol-1 | D. | △H1<△H3 |
20.能正确表示下列反应的离子方程式的是( )
| A. | 用过量氨水吸收工业尾气中的SO2:2NH3•H2O+SO2═2NH4++SO32-+H2O | |
| B. | 氯化钠与浓硫酸混合加热:H++Cl-$\frac{\underline{\;\;△\;\;}}{\;}$HCl↑ | |
| C. | 磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+3H2O | |
| D. | 明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀:2Ba2++3OH-+Al3++2SO42-═2BaSO4↓+Al(OH)3↓ |
17.铜及其化合物在工农业生产及日常生活中应用非常广泛.回答下列问题:
(1)纳米级Cu2O由于具有优良的催化性能而受到关注,制取Cu2O的两种方法如表所示.
①方法I中还原剂与氧化剂的物质的量之比为1:4.
②方法II发生反应的化学方程式为4Cu(OH)2+N2H4=Cu2O+N2↑+6H2O.
(2)氢化亚铜是一种红色同体,可由下列反应制备:4CuSO4+3H3PO2+6H2O=4CuH↓+4H2SO4+3H3PO4
该反应中每转移3mol电子,生成CuH的物质的量为1mol.
(3)氯化铜溶液中各种含铜微粒的分布分数(平衡时某微粒的浓度占各微粒浓度之和的分数)与c(C1-)之间的关系如图所示.
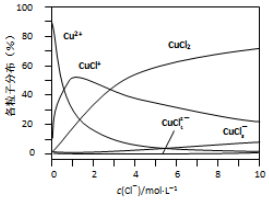
①当c(C1-)=9mol/L时,溶液中3种主要含铜微粒浓度的大小关系为c(CuCl2)>c(CuCl+)>c(CuCl3-).
②在c(C1-)=l mol/L的氯化铜溶液中,加人AgNO3溶液,CuCl+转化为Cu2+的离子方程式为CuCl++Ag+=Cu2++AgCl↓.
(4)已知:Cu(OH)2是二元弱碱,25℃时Ksp=2.0×10-20.则此温度下在铜盐溶液中Cu2+发生水解反应的平衡常数为5×10-9.
(1)纳米级Cu2O由于具有优良的催化性能而受到关注,制取Cu2O的两种方法如表所示.
| 方法I | 用炭粉在高温条件下还原CuO生成Cu2O和CO2 |
| 方法II | 用肼(N2H4)还原新制Cu(OH)2 |
②方法II发生反应的化学方程式为4Cu(OH)2+N2H4=Cu2O+N2↑+6H2O.
(2)氢化亚铜是一种红色同体,可由下列反应制备:4CuSO4+3H3PO2+6H2O=4CuH↓+4H2SO4+3H3PO4
该反应中每转移3mol电子,生成CuH的物质的量为1mol.
(3)氯化铜溶液中各种含铜微粒的分布分数(平衡时某微粒的浓度占各微粒浓度之和的分数)与c(C1-)之间的关系如图所示.

①当c(C1-)=9mol/L时,溶液中3种主要含铜微粒浓度的大小关系为c(CuCl2)>c(CuCl+)>c(CuCl3-).
②在c(C1-)=l mol/L的氯化铜溶液中,加人AgNO3溶液,CuCl+转化为Cu2+的离子方程式为CuCl++Ag+=Cu2++AgCl↓.
(4)已知:Cu(OH)2是二元弱碱,25℃时Ksp=2.0×10-20.则此温度下在铜盐溶液中Cu2+发生水解反应的平衡常数为5×10-9.
18.化学与生活、生产、环境密切相关. 下列说法不正确的是( )
| A. | 工厂排放 CO2会导致酸雨的形成 | |
| B. | 使用含有氯化钙的融雪剂会加速桥梁的腐蚀 | |
| C. | “山东疫苗案”涉及疫苗未冷藏储运而失效,这与蛋白质变性有关 | |
| D. | 《黄白第十六》中有“曾青涂铁,铁赤如铜”,这与化学变化有关 |



