题目内容
 硼是新型无机材料中的明星元素.
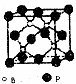
硼是新型无机材料中的明星元素.(1)磷化硼是一种的耐磨涂料,图为磷化硼晶体结构中最小的重复结构单元.磷化硼的晶体类型是
(2)氮化硼是一种重要的功能陶瓷材料,B和N相比,电负性较大的是
(3)环硼氮烷与苯是等电子体.写出其分子结构式
(4)BF3用作有机合成中的催化剂,也用于制造火箭的高能燃料.在BF3分子中,F-B-F的键角是
考点:不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:(1)根据其空间结构确定晶体类型,利用均摊法计算原则数目;
(2)N原子核外电子数目为7,根据核外电子排布规律书写;同周期从左到右电负性依次增强,B第IIIA族元素,为+3价;
(3)根据苯的结构确定环硼氮烷的结构简式;
(4)价层电子对互斥理论认为:分子的立体构型是“价层电子对”相互排斥的结果,先判断价层电子对数,再确定构型和杂化方式;
(2)N原子核外电子数目为7,根据核外电子排布规律书写;同周期从左到右电负性依次增强,B第IIIA族元素,为+3价;
(3)根据苯的结构确定环硼氮烷的结构简式;
(4)价层电子对互斥理论认为:分子的立体构型是“价层电子对”相互排斥的结果,先判断价层电子对数,再确定构型和杂化方式;
解答:
解:(1)根据其根据结构知,该物质为空间网状结构,所以是原子晶体,晶胞中原子数=8×
+6×
=4;
故答案为:原子晶体;4;
(2)N原子核外电子数目为7,原子的电子排布式为1s22s22p3,同周期从左到右电负性依次增强,所以电负性N>B;B第ⅢA族元素,为+3价;
故答案为:N;1s22s22p3;+3;
(3)根据苯的结构确定环硼氮烷的结构简式为: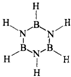 ;
;
故答案为: ;
;
(4)BF3分子的中心原子B原子上含有3个σ 键,中心原子上的孤电子对数=
(a-xb)=
(0-3×1)=0,所以BF3分子的VSEPR模型是平面三角型,中心原子上没有孤对电子,所以其空间构型就是平面三角形,键角是120°,BF3分子的中心原子B原子的价层电子对数为;3,属于sp2杂化;
BF3和过量NaF作用可生成NaBF4,BF4-中B原子的价层电子对4+
=4,该离子中不含孤电子对,为正四面体结构.正四面体;
故答案为:120°;sp2杂化;正四面体.
| 1 |
| 8 |
| 1 |
| 2 |
故答案为:原子晶体;4;
(2)N原子核外电子数目为7,原子的电子排布式为1s22s22p3,同周期从左到右电负性依次增强,所以电负性N>B;B第ⅢA族元素,为+3价;
故答案为:N;1s22s22p3;+3;
(3)根据苯的结构确定环硼氮烷的结构简式为:
 ;
;故答案为:
 ;
;(4)BF3分子的中心原子B原子上含有3个σ 键,中心原子上的孤电子对数=
| 1 |
| 2 |
| 1 |
| 2 |
BF3和过量NaF作用可生成NaBF4,BF4-中B原子的价层电子对4+
| 3+1-1×4 |
| 2 |
故答案为:120°;sp2杂化;正四面体.
点评:本题考查了物质结构的综合性知识,原子的杂化方式、分子的空间构型、键角等知识点是高考的热点,应重点掌握,难度中等.

练习册系列答案
相关题目
下列各组物质不属于同分异构体的是( )
| A、2-甲基丁烷和戊烷 |
| B、乙二醇和丙三醇 |
| C、2,2-二甲基-1-丙醇和2-甲基-2-丁醇 |
| D、苯甲醇和对甲基苯酚 |
化学在生产和日常生活中有着重要的应用.下列叙述正确的是( )
| A、氯气是合成塑料、橡胶、农药和制盐酸、有机溶剂的重要原料 |
| B、“辽宁舰”上用于舰载机降落拦阻索的特种钢缆,属于新型无机非金属材料 |
| C、白酒中混有少量塑化剂,少量饮用对人体无害,可通过过滤方法除去 |
| D、“雾霾天气”、“温室效应”、“光化学烟雾”的形成都与氮氧化物无关 |
下列反应中属于吸热反应的是( )
| A、活泼金属与酸反应 |
| B、Ba(OH)2?8H2O晶体与NH4Cl晶体的反应 |
| C、酸碱中和反应 |
| D、镁条燃烧 |
中学化学课本中有大量的数据资料.下面是某学生对数据的利用.其中不正确的是( )
| A、利用相对分子质量大小可以判断某些物质的熔沸点高低 |
| B、利用密度数据可判断液体物质挥发性的大小 |
| C、利用原子(或离子)半径数据可推断某些原子(或离子)的氧化性和还原性的强弱 |
| D、利用溶解度数据可推测将一些物质混合物分离开来的可能性 |
能正确表示下列反应的离子方程式是( )
| A、硫酸铝溶液中加入过量烧碱:Al3++3OH-=Al(OH)3↓ |
| B、碳酸钠溶液中加入醋酸:CO32-+2H+=CO2↑+H2O |
| C、碳酸氢钠溶液中加入氢氧化钠:HCO3-+OH-=CO32-+H2O |
| D、常温时,浓硝酸中加入铁片:Fe+6H++3NO3-=Fe3++3NO2↑+3H2O |
 酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题: