题目内容
下列排序正确的是( )
| A、微粒半径:Fe(OH)3胶粒<K+<S2- |
| B、热稳定性:PH3<NH3<H2O |
| C、碱性:Mg(OH)2<Al(OH)3<NaOH |
| D、熔点:CaCl2<SO3<SiC |
考点:元素周期律的作用
专题:元素周期律与元素周期表专题
分析:A.离子半径小于胶体粒子半径;具有相同排布的离子原子序数大的离子半径小;
B.非金属性越强,气态氢化物越稳定;
C.元素的金属性越强,最高价氧化物的水化物的碱性越强;
D.一般来说,晶体的熔点:原子晶体>离子晶体>金属晶体.
B.非金属性越强,气态氢化物越稳定;
C.元素的金属性越强,最高价氧化物的水化物的碱性越强;
D.一般来说,晶体的熔点:原子晶体>离子晶体>金属晶体.
解答:
解:A.离子半径小于胶体粒子半径;具有相同排布的离子原子序数大的离子半径小,则微粒半径为Fe(OH)3胶粒>S2->K+,故A错误;
B.非金属性O>N>P,故气态氢化物的稳定性为H2O>NH3>PH3,故B正确;
C.元素的金属性越强,对应最高价氧化物的水化物的碱性越强,金属性:Al<Mg<Na,故碱性:Al(OH)3<Mg(OH)2<NaOH,故C错误;
D.一般来说,晶体的熔点:原子晶体>离子晶体>金属晶体,所以熔点:SO3<CaCl2<SiC,故D错误;
故选B.
B.非金属性O>N>P,故气态氢化物的稳定性为H2O>NH3>PH3,故B正确;
C.元素的金属性越强,对应最高价氧化物的水化物的碱性越强,金属性:Al<Mg<Na,故碱性:Al(OH)3<Mg(OH)2<NaOH,故C错误;
D.一般来说,晶体的熔点:原子晶体>离子晶体>金属晶体,所以熔点:SO3<CaCl2<SiC,故D错误;
故选B.
点评:本题考查元素性质的递变规律以及晶体熔点的比较,难度不大.注意金属性和非金属性与对应单质、化合物的性质的关系.

练习册系列答案
相关题目
航天飞机用铝粉与高氯酸铵(NH4ClO4)的混合物为固体燃料,点燃时铝粉氧化放热引发高氯酸铵反应,其方程式可表示为:2NH4ClO4
N2↑+4H2O+Cl2↑+2O2↑+Q.下列对此反应的叙述中错误的是( )
| △ |
| A、上述反应中,每生成1molN2则转移电子6mol |
| B、上述反应瞬间产生大量高温气体推动航天飞机飞行 |
| C、反应从能量变化上说,主要是化学能转变为热能和动能 |
| D、在反应中高氯酸铵既起氧化剂,又起还原剂作用 |
下列溶液中,跟100mL 0.5mol/L NaCl溶液所含的氯离子物质的量浓度相同的是( )
| A、100mL 0.5 mol/L MgCl2溶液 |
| B、25 mL 0.5mol/L HCl溶液 |
| C、50 mL 1mol/L NaCl溶液 |
| D、200 mL 0.25mol/L CaCl2溶液 |
下列电离方程式中,正确的是( )
| A、H2S?2H++S2- |
| B、NaHCO3═Na++H++CO32- |
| C、K2SO4═2K++SO42- |
| D、NH3?H2O═NH4++H2O |
下列各组物质中,物质之间通过一步反应就能实现图示转化的是( )
| 物质编号 | 物质转化关系 | a | b | c | d |
| ① | 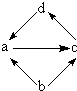 | FeCl2 | Fe | FeCl3 | CuCl2 |
| ② | Na2O | Na | Na2O2 | Mg(OH)2 | |
| ③ | NO | N2 | NO2 | NaCl | |
| ④ | Al2O3 | Al | Na[Al(OH)4] | Al(OH)3 |
| A、①②③ | B、①③④ |
| C、①④ | D、②④ |
短周期元素X、Y、Z、W、Q的原子序数依次增大,且只有一种金属元素.其中X与W处于同一主族,Z元素原子半径在短周期中最大(稀有气体除外).W、Z之间与W、Q之间原子序数之差相等,五种元素原子最外层电子数之和为21,下列说法正确的是( )
| A、Y的简单离子半径小于Z的简单离子半径 |
| B、Z最高价氧化物对应的水化物分别与X、Y最高价氧化物对应的水化物反应生成1mol水时所放出的热量相同 |
| C、Y的简单气态氢化物在一定条件下可被Q单质氧化 |
| D、Q可分别与X、Y、Z、W形成化学键类型相同的化合物 |