题目内容
将充有n mLNO和m mLNO2气体的试管倒立于盛水的水槽中,然后通入n mLO2.m>n,则充分反应后,试管中气体在同温同压下的体积为( )A.
 mL
mLB.
 mL
mLC.
 mL
mLD.
 mL
mL
【答案】分析:先根据反应3NO2+2H2O=2HNO3+NO,求出所有的NO,再根据反应4NO+3O2+2H2O=4HNO3,求出剩余气体的体积.
解答:解:根据反应可知
3NO2 +2H2O=2HNO3 +NO,
3 1
m m
m
所以反应后NO气体共(n+ m)mL,
m)mL,
设消耗的氧气的体积为x,
由4NO+3O2 +2H2O=4HNO3,
4 3
(n+ m) x
m) x
x=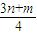 ,
,
由m>n可知,x>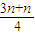 =n,
=n,
显然氧气不足,完全反应,
剩余气体为NO,NO的体积为(n+ m)mL-
m)mL- nmL=
nmL=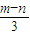 mL,
mL,
故选A.
点评:本题考查氮的氧化物与水的反应,明确发生的化学反应及m、n的关系是解答本题的关键,熟悉体积与物质的量成正比即可解答.
解答:解:根据反应可知
3NO2 +2H2O=2HNO3 +NO,
3 1
m
 m
m 所以反应后NO气体共(n+
 m)mL,
m)mL,设消耗的氧气的体积为x,
由4NO+3O2 +2H2O=4HNO3,
4 3
(n+
 m) x
m) xx=
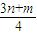 ,
,由m>n可知,x>
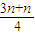 =n,
=n,显然氧气不足,完全反应,
剩余气体为NO,NO的体积为(n+
 m)mL-
m)mL- nmL=
nmL=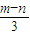 mL,
mL,故选A.
点评:本题考查氮的氧化物与水的反应,明确发生的化学反应及m、n的关系是解答本题的关键,熟悉体积与物质的量成正比即可解答.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目