题目内容
下列事实合理,且能用勒夏特列原理解释的是( )
| A、实验室用排饱和食盐水法收集少量氯气 |
| B、对2HI?H2+I2(g)平衡体系增加压强使颜色变深 |
| C、反应CO+NO2?CO2+NO 正反应放热,升高温度使平衡向正方向移动 |
| D、氢能是目前世界上比较理想的能源之一 |
考点:化学平衡移动原理
专题:化学平衡专题
分析:勒夏特列原理为:如果改变影响平衡的条件之一,平衡将向着能够减弱这种改变的方向移动.使用勒夏特列原理时,该反应必须是可逆反应,否则勒夏特列原理不适用.
解答:
解:A.氯气和水反应生成氯化氢和次氯酸,是化学平衡,饱和氯化钠溶液中氯离子浓度大,平衡逆向进行,降低氯气溶解度,能用勒夏特列原理解释,故A正确;
B.对2HI?H2+I2(g)平衡体系,反应前后气体体积不变,增加压强,体积减小,平衡不动,使气体颜色变深,不能用勒夏特列原理解释,故B错误;
C.反应CO+NO2?CO2+NO正反应放热,升高温度使平衡向逆方向移动,不符合事实,故C错误;
D.氢气燃烧生成水,所以氢能是目前世界上比较理想的能源之一,但是与勒夏特列原理无关,故D错误;
故选A.
B.对2HI?H2+I2(g)平衡体系,反应前后气体体积不变,增加压强,体积减小,平衡不动,使气体颜色变深,不能用勒夏特列原理解释,故B错误;
C.反应CO+NO2?CO2+NO正反应放热,升高温度使平衡向逆方向移动,不符合事实,故C错误;
D.氢气燃烧生成水,所以氢能是目前世界上比较理想的能源之一,但是与勒夏特列原理无关,故D错误;
故选A.
点评:本题考查了化学平衡移动原理应用,题目难度中等,明确平衡移动原理的内容是解题关键,注意掌握化学平衡及其影响因素,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、饱和石灰水中加入少量CaO,恢复至室温后溶液的pH不变 |
| B、稀醋酸加水稀释,醋酸电离程度增大,溶液pH减小 |
| C、盐酸中滴加氨水呈中性,溶液中的溶质为氯化铵 |
| D、向沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强 |
下列说法正确的是( )
| A、制作航天服的聚酯纤维和用于光缆通信的晶体硅都是新型无机非金属材料 |
| B、煤经过干馏加工可变为汽油柴油等能源 |
| C、石油化工生产中广泛使用过渡元素做催化剂并加入少量稀土元素改善催化剂的性能 |
| D、红宝石、水晶、钻石的主要成分都是硅酸盐 |
下列变化必须加入还原剂才能实现的是( )
| A、N2→NH3 |
| B、Zn→Zn2+ |
| C、H2→H2O |
| D、CuO→CuCl2 |
H-是负一价的阴离子,它可与NH3发生以下反应:H-+NH3=H2+NH2-,下列有关这个反应的说法中正确的是( )
| A、它属于置换反应 |
| B、该反应中NH2-是还原产物 |
| C、该反应中NH3被氧化 |
| D、反应中被氧化和被还原的元素都是H元素 |

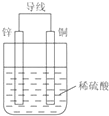 根据铜锌原电池示意图,回答下列问题:
根据铜锌原电池示意图,回答下列问题: