题目内容
19.下列叙述正确的是( )| A. | 铝粉与氧化镁共热可制取金属镁 | |
| B. | 铝分别与足量的 HCl溶液、足量的NaOH的溶液反应,产生的氢气前者多 | |
| C. | 氯化汞(HgCl2)的稀溶液可用于手术器械消毒,因为它会使蛋白质变性,杀菌消毒 | |
| D. | NaOH溶液可以盛装在带玻璃塞的磨口试剂瓶中 |
分析 A.Mg为活泼金属,还原性大于Al;
B.HCl、NaOH均完全反应,由2Al~6HCl~2NaOH~3H2↑分析;
C.氯化汞为重金属盐,可使蛋白质变性;
D.玻璃塞的磨口试剂瓶,氢氧化钠易与玻璃成分SiO2酸性氧化物反应.
解答 解:A.Mg为活泼金属,还原性大于Al,铝粉与氧化镁不反应,电解熔融氯化镁冶炼Mg,故A错误;
B.HCl、NaOH均完全反应,由2Al~6HCl~2NaOH~3H2↑可知,铝分别与足量的 HCl溶液、足量的NaOH的溶液反应,产生的氢气物质的量比为1:1,故B错误;
C.氯化汞为重金属盐,可使蛋白质变性,稀溶液可用于杀菌消毒,故C正确;
D.NaOH溶液的存放方法是:密封保存,试剂瓶应用橡胶塞或软木塞,不能用玻璃塞,因为NaOH能与玻璃中的SiO2反应,化学方程式为:2NaOH+SiO2=Na2SiO3+H2O,故D错误.
故选C.
点评 本题考查较为综合,涉及金属冶炼、蛋白质变性、试剂的保存等知识,有利于培养学生良好的科学素养,提高学习的积极性,题目难度不大,注意相关基础知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.Q、W、X、Y、Z是原子序数依次增大的短周期主族元素,Q、Y在周期表中相对位置如下:
已知:Q元素最低负化合价的绝对值与其原子最外层电子数相等,W、Y同主族,X是地壳中含量最多的金属元素.下列说法正确的是( )
| Q | ||||
| Y |
| A. | Q的最高价氧化物属于离子化合物 | |
| B. | W和氢元素组成的化合物分子中只含有极性共价键 | |
| C. | Q、X、Y、Z元素最高价氧化物对应的水化物中酸性最强的是HZO4 | |
| D. | 工业上可用电解熔融的X的氯化物方法来制备X单质 |
10.T℃时,在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g).反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Z的百分含量与时间的关系如图2所示.则下列结论正确的是( )
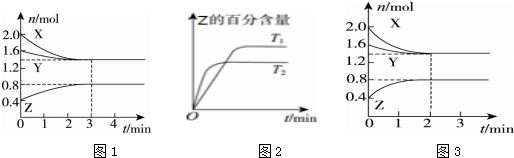

| A. | 容器中发生的反应可表示为3X(g)+Y(g)═2Z(g) | |
| B. | 反应进行的前3 min内,用X表示的反应速率v(X)=0.2 mol/(L•min) | |
| C. | 保持其他条件不变,升高温度,反应的化学平衡常数K减小 | |
| D. | 若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强 |
7.下列化学用语表述正确的是( )
| A. | 羟基的电子式: | B. | 硝基苯的结构简式: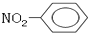 | ||
| C. | 四氯化碳的球棍模型: | D. | NH4Br的电子式: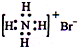 |
4.下列关于物质性质或检验的叙述不正确的是( )
| A. | 在溶液中加KSCN,溶液显红色,不能证明原溶液中一定有Fe3+,无Fe2+ | |
| B. | 气体通过湿润的红色石蕊试纸,试纸变蓝,证明原气体中一定含有氨气 | |
| C. | 用铂丝灼烧白色粉末,火焰成黄色,证明原粉末中一定有Na+,可能有K+ | |
| D. | 向某溶液中加盐酸产生无色气体,该气体能使澄清的石灰水变浑浊,说明该溶液中一定含有CO32-或SO32- |
11.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,2.24 L NO2溶于水完全反应转移电子数为0.2NA | |
| B. | 标准状况下,5.6L二氧化碳气体中含有的氧原子数为0.5NA | |
| C. | 氢原子数为0.6NA的乙烯分子中含有的π键数为0.2NA | |
| D. | 0.1L0.5mol/LCH3COOH溶液中含有的氢离子数为0.05NA |
8.下列关于价电子构型3s23p4的描述正确的是( )
| A. | 该元素的电负性是同主族最大的 | |
| B. | 其轨道表示式为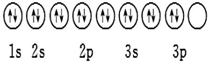 | |
| C. | 可以与H2化合生成液态化合物 | |
| D. | 它的核外电子排布式为1s22s22p63s23p4 |
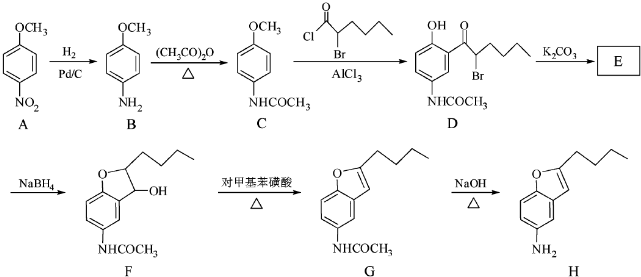
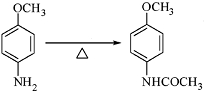 +CH3COOH
+CH3COOH .
.