题目内容
5.用阳极a和阴极b电解c的水溶液一段时间,然后加入d,能使溶液恢复到电解前状态,a、b、c、d正确组合是( )| 选项 | a | b | c | d |
| A | Pt | Pt | NaOH | NaOH |
| B | C | C | NaCl | NaOH |
| C | Cu | Cu | CuSO4 | Cu(OH)2 |
| D | Pt | Pt | H2SO4 | H2O |
| A. | A | B. | B | C. | C | D. | D |
分析 用b作阴极,a作阳极,电解c的水溶液,电解一段时间后,再加入d能使溶液恢复到电解前的状态,应首先根据电解原理确定两个电极反应,并判断电解产物,要满足溶液浓度不变,根据“出什么加什么”来确定加入的物质.
解答 解:A、电解NaOH溶液实际上是电解的水,加入一定量的水可恢复原浓度,故A错误;
B、电解食盐水,生成NaOH、H2、Cl2,加盐酸显然不能恢复电解前的状态,应通入适量的HCl气体,故B错误;
C、阴极上是铜离子得电子的反应,产生金属铜,阳极是铜放电,则溶液浓度不变,加入CuSO4则CuSO4浓度增大,故C错误;
D、电解硫酸溶液实际上是电解的水,加入一定量的水可恢复原浓度,故D正确;
故选D.
点评 本题考查电解原理,解答本题要注意把握两极的反应,注意要满足溶液浓度不变,应再加入电解产物,学习中注意把握电解原理和阴阳离子的放电顺序,题目难度不大.

练习册系列答案
相关题目
12.如图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中,下列分析正确的是( )


| A. | K1、K2闭合时,Na+均移向铁棒 | |
| B. | K1闭合,石墨棒周围溶液pH逐渐升高 | |
| C. | K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法 | |
| D. | K2闭合,电路中通过0.4NA个电子时,两极共产生标况下4.48L气体 |
13.7瓶分别含有Cu2+、Fe3+、A13+、Mg2+、Fe2+、NH4+、Na+等离子的溶液,只用一种试剂即可鉴别,该试剂是( )
| A. | KMnO4溶液 | B. | KSCN溶液 | C. | NaOH溶液 | D. | NH3•H2O溶液 |
13.有人曾建议用 AG 表示溶液的酸度,AG 的定义为:AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$,室温下实验室用0.01mol?L-1 的氢氧化钠溶液滴定 20mL 相同浓度的醋酸溶液,滴定曲线如图所示.下列有关叙述正确的是( )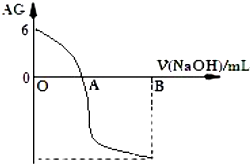

| A. | A 点时加入氢氧化钠溶液体积为 20 mL | |
| B. | OA 段溶液中:c(CH3COO-)>c(CH3COOH) | |
| C. | 室温时 0.01 mol/L的醋酸溶液 pH=4 | |
| D. | 若 B 点时加入 NaOH 溶液为 40 mL,所得溶液中:c(CH3COO-)+c(CH3COOH)=c(OH-) |
20.将2mol/L HCN溶液和1mol/L NaOH溶液等体积混合后,溶液显碱性,下列关系式中正确的是( )
| A. | c(HCN)>c(CN-) | B. | c(Na+)<c(CN-) | ||
| C. | c(HCN)-c(CN-)=c(OH-) | D. | c(HCN)+c(CN-)=2 mol/L |
10.下列说法正确的是( )
| A. | 将0.2 mol/L的一元酸HA溶液和0.1 mol/L的NaOH溶液混合,混合液中一定有:c(OH-)+c(A-)=c(H+)+c(Na+) | |
| B. | 某溶液中由水电离出的c(OH-)=1×10-9mol/L,则该溶液的pH一定为5 | |
| C. | 室温下,NaHSO3溶液的pH<7,则溶液中c(SO32-)<c(H2SO3) | |
| D. | Na2CO3溶液与NaHCO3溶液混合一定有2c(Na+)=3[c(CO32-)+c(HCO3-)+c(H2CO3)] |
14.将足量的MnO2与含14.6gHCl的浓盐酸共热制取氯气,可制得Cl2的质量是( )
| A. | 等于7.1g | B. | 小于7.1g | ||
| C. | 大于7.1g,小于14.2g | D. | 大于14.2g |