题目内容
11.已知合成氨反应的浓度数据如下:3H2+N2?$?_{高温高压}^{催化剂}$ 2NH3| 起始浓度/mol•L-1 | 3 | 1 | 0 |
| 2s末浓度/mol•L-1 | 1.8 | 0.6 | 0.8 |
| A. | 0.4 mol•L-1•s-1 | B. | 0.2 mol•L-1•s-1 | C. | 0.8 mol•L-1•s-1 | D. | 0.6 mol•L-1•s-1 |
分析 根据表中数据可知,起始浓度为0、2s末浓度为0.8mol/L的表示的是氨气的浓度变化,然后根据v=$\frac{△c}{△t}$计算出用NH3的浓度的增加来表示该反应的反应速率.
解答 解:第1、2组反应物浓度都减小,只有第三组的浓度增加,则氨气的浓度增加为:0.8mol/L,
所以用NH3的浓度的增加来表示该反应的反应速率为:v(NH3)=$\frac{0.8mol/L}{2s}$=0.4 mol•L-1•s-1,
故选A.
点评 本题考查了化学反应速率的计算,题目难度不大,根据浓度变化正确判断反应物、生成物的浓度变化为解答关键,注意掌握化学反应速率的表达式,试题培养了学生的化学计算能力.

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
2.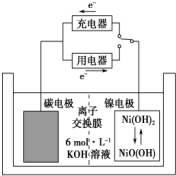 一种碳纳米管能够吸附氢气,可作二次电池(如图所示)的碳电极.该电池的电解质溶液为6mol•L-1的KOH溶液,下列说法中不正确的是( )
一种碳纳米管能够吸附氢气,可作二次电池(如图所示)的碳电极.该电池的电解质溶液为6mol•L-1的KOH溶液,下列说法中不正确的是( )
 一种碳纳米管能够吸附氢气,可作二次电池(如图所示)的碳电极.该电池的电解质溶液为6mol•L-1的KOH溶液,下列说法中不正确的是( )
一种碳纳米管能够吸附氢气,可作二次电池(如图所示)的碳电极.该电池的电解质溶液为6mol•L-1的KOH溶液,下列说法中不正确的是( )| A. | 充电时阴极反应:2H2O+2e-═2OH-+H2↑ | |
| B. | 充电时将碳电极与电源的负极相连 | |
| C. | 放电时,OH-移向碳电极 | |
| D. | 放电时镍电极反应为:Ni(OH)2+OH--e-═NiO(OH)+H2O |
3.下列所述反应的方程式或关系式正确的是( )
| A. | 常温下,0.1 mol•L-1 HA溶液的pH=3,则HA的电离:HA=H++A- | |
| B. | 向硫酸铵溶液中加入适量氨水,当溶液呈酸性时,溶液中c(SO42-)=c(NH4+) | |
| C. | 向1 mL 2 mol•L-1NaOH溶液中滴加1~2滴0.1 mol•L-1MgCl2溶液后,再滴加2滴0.1 mol•L-1 FeCl3溶液:Mg2++2OH-=Mg(OH)2↓,3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ | |
| D. | 浓度相等的①NH4HSO4②NH4C1③(NH4)2SO4溶液中,c(NH4+)的大小顺序为③>①>② |
1.下列各组物质,具有相同的最简式,但既不属于同分异构体又不属于同系物的是( )
①聚乙烯和乙烯 ②甲醛和葡萄糖 ③淀粉和纤维素 ④蔗糖和麦芽糖 ⑤聚乙烯和聚氯乙烯.
①聚乙烯和乙烯 ②甲醛和葡萄糖 ③淀粉和纤维素 ④蔗糖和麦芽糖 ⑤聚乙烯和聚氯乙烯.
| A. | ①②⑤ | B. | ①②③ | C. | ①④⑤ | D. | ①②③⑤ |
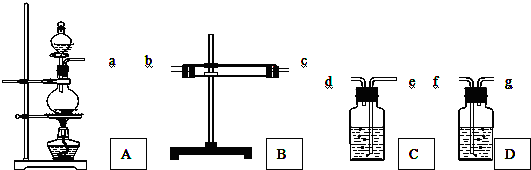
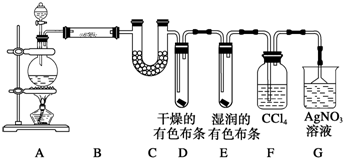 某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题.
某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题.