题目内容
17.同周期或同主族元素中,不仅元素的基本性质呈周期性变化,而且它们的单质和化合物的性质也有一定的变化规律.(1)在“比较钠、镁、铝金属活泼性”实验中,甲、乙两组的实验如下:
| 甲 组 | 乙 组 | ||
| 实验步骤 | 实验现象 | 实验步骤 | 实验现象 |
| 1.取两支试管,加入3mL水,各滴入2滴酚酞试液,分别加入一小粒金属钠和少量镁粉,观察现象. 将加入镁粉的试管加热至沸腾,观察现象. | 钠:在冷水中,浮于水面,熔成小球,四处游动,逐渐缩小,溶液很快变红色. 镁:在冷水中几乎无现象,加热至沸后产生大量气体,溶液变红. | 1.取两支试管,加入3mL水,各滴入2滴酚酞试液,分别加入一小粒金属钠和少量镁粉,观察现象. 将加入镁粉的试管加热至沸腾,观察现象. | 钠:在冷水中,浮于水面,熔成小球,四处游动,逐渐缩小,溶液很快变红色. 镁:在冷水中几乎无现象,加热至沸后产生大量气体,溶液变红. |
| 2.取一小块铝和一小块镁带,用砂纸擦去表面的氧化膜,分别同时投入盛有2mL1mol/L盐酸的两个试管中,观察现象. | 镁:剧烈反应,很快产生大量气体. 铝:也产生大量气体,但反应比镁慢. | 2.取一小块铝和一小块镁带,分别同时投入盛有2mL1mol/L盐酸的两个试管中,观察现象. | 镁:开始时没有现象,过一会儿产生大量气体. 铝:基本没有变化. |
②写出铝和盐酸反应的离子方程式2Al+6H+═2Al3++3H2↑.
③钠、镁、铝金属活泼性由强到弱顺序是钠、镁、铝;甲、乙两组中,乙组的实验更可靠,另一组不可靠的原因没有除去金属表面的氧化膜,氧化铝性质稳定不易与酸反应.
(2)同周期元素中,氯比硫的非金属性强,下列叙述中不能证明这一事实的是BD.
A.向新制的饱和硫化氢溶液中通入氯气会产生淡黄色沉淀
B.常温时,氯气是气体,硫是固体
C.氯的最高价氧化物对应水化物的酸性比硫的强
D.氯气和硫分别跟氢气反应,生成的氢化物中氯和硫的化合价分别为-1、-2.
分析 (1)①钠和水反应生成氢氧化钠和氢气;
②铝和盐酸反应生成氯化铝和氢气,反应的离子方程式2Al+6H+═2Al3++3H2↑;
③钠:在冷水中,浮于水面,熔成小球,四处游动,逐渐缩小,溶液很快变红色;镁:在冷水中几乎无现象,加热至沸后产生大量气体,溶液变红,钠比镁与水反应剧烈,所以钠比镁,而镁:剧烈反应,很快产生大量气体;铝:也产生大量气体,但反应比镁慢,镁与酸反应比铝剧烈,所以镁比铝活泼,综上所述活泼性由强到弱顺序是:钠>镁>铝;铝是活泼的金属,表面极易被氧化,形成致密的氧化膜;
(2)利用非金属与氢气化合的难易程度、气态氢化物的稳定性、最高价氧化物的水化物的酸性、非金属单质之间的置换反应等来判断非金属性的强弱,以此来解答.
解答 解:(1)①钠和水反应生成氢氧化钠和氢气,反应的化学方程式2Na+2H2O═2NaOH+H2↑,故答案为:2Na+2H2O═2NaOH+H2↑;
②铝和盐酸反应生成氯化铝和氢气,反应的离子方程式2Al+6H+═2Al3++3H2↑,故答案为:2Al+6H+═2Al3++3H2↑;
③钠:在冷水中,浮于水面,熔成小球,四处游动,逐渐缩小,溶液很快变红色;镁:在冷水中几乎无现象,加热至沸后产生大量气体,溶液变红,钠比镁与水反应剧烈,所以钠比镁,而镁:剧烈反应,很快产生大量气体;铝:也产生大量气体,但反应比镁慢,镁与酸反应比铝剧烈,所以镁比铝活泼,综上所述活泼性由强到弱顺序是:钠>镁>铝;铝是活泼的金属,表面极易被氧化,形成致密的氧化膜,所以甲组的实验更可靠,故答案为:钠、镁、铝;乙;没有除去金属表面的氧化膜,氧化铝性质稳定不易与酸反应;
(2)A.由氯气与H2S的水溶液反应生成S,则Cl的非金属性比S的强,故A正确;
B.常温时,氯气是气体,硫是固体,无法说明非金属性的强弱,故B错误;
C.氯的最高价氧化物对应水化物的酸性比硫的强,非金属越强,所以氯比硫的非金属性强,故C正确;
D.氯气和硫分别跟氢气反应,生成的氢化物中氯和硫的化合价分别为-1、-2,化合价与最外层电子数有关,所以不能直接根据最外层电子数多少判断比较非金属性的强弱,故D错误.
故选BD.
点评 本题考查金属和非金属性的比较,题目难度不大,注意归纳非金属性比较的常见方法即可解答,注重规律性知识的应用来解答.

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案| A. | CH4 | B. | SO2 | C. | NO | D. | NO2 |
| A. | BaCl2溶液 | B. | 品红溶液 | C. | 盐酸 | D. | NH4Cl |
| A. | O2在放电条件下变成O3 | B. | 加热胆矾成无水硫酸铜 | ||
| C. | 漂白的草帽久置于空气中变黄 | D. | 石油分馏 |
| A. | 1 mol聚乙烯含有的原子数目为6NA | |
| B. | 标准状况下,11.2L CHCl3中所含有的原子总数为2.5NA | |
| C. | 一定条件下,2.6 g乙炔、苯和苯乙烯的气态混合物中所含碳原子数为0.2NA | |
| D. | 1 mol甲基含10 NA个电子 |
(1)下列关于氯水的叙述正确的是aef(填写符号).
a.氯水中存在两种电离平衡
b.向氯水中通入SO2,其漂白性增强
c.向氯水中通入氯气,c(H+)/c(ClO-)减小
d.加水稀释氯水,溶液中的所有离子浓度均减小
e.加水稀释氯水,水的电离平衡向正反应方向移动
f.向氯水中加入少量固体NaOH,可能有c(Na+)=c(Cl-)+c(ClO-)
(2)常温下,已知25℃时有关弱酸的电离平衡离数:
| 弱酸化学式 | HClO | H2CO3 |
| 电离平衡常数 | 4.7×10-8 | K1=4.3×10-7 K2=5.6×10-11 |
(3)电解饱和食盐水可得到溶质为M的碱溶液,常温下将浓度为c1的M溶液与0.1mol•L-1的一元酸HA等体积混合,所得溶液pH=7,则c1≤ 0.1mol•L-1(填“≥”、“≤”或“=”),溶液中离子浓度的大小关系为c(Na+)=c(A-)>c(OH-)=c(H+).若将上述“0.1mol•L-1的一元酸HA”改为“pH=1的一元酸HA”,所得溶液的pH仍为7,则c1≥0.1mol•L-1.
(4)牙釉质对牙齿起着保护作用,其主要成分为羟基磷灰石(Ca5(PO4)3OH),研究证实氟磷灰石(Ca5(PO4)3F)比它更能抵抗酸的侵蚀,故含氟牙膏已使全世界千百万人较少龋齿,请写出羟基磷灰石的溶度积常数表达式Ksp=c5(Ca2+)c3(PO43-)c(OH-),氟离子与之反应转化的离子方程式为Ca5(PO4)3OH+F-═Ca5(PO4)3F+OH-.
| A. | LiAlH4与乙醛作用生成乙醇,LiAlH4作还原剂 | |
| B. | LiAlH4与D2O反应,所得氢气的摩尔质量为4 g•mol-1 | |
| C. | 1 mol LiAlH4在125℃完全分解,转移3 mol电子 | |
| D. | LiAlH4与水反应生成三种物质时,化学方程式可表示为:LiAlH4+4H2O═Al(OH)3↓+LiOH+4H2↑ |
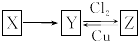 X、Y、Z是中学化学中常见的单质或化合物,且X、Y、Z均含有同一种元素,它们能实现如图所示的转化关系(其他物质省略):
X、Y、Z是中学化学中常见的单质或化合物,且X、Y、Z均含有同一种元素,它们能实现如图所示的转化关系(其他物质省略):