题目内容
10.已知X、Y、Z三种醇互为同系物,则建立在假设基础上的推断正确的是( )| 假设 | 推断 | |
| A | 若X、Y均能发生消去反应 | Z一定能发生消去反应 |
| B | 若X是白酒的主要成分 | Y可能是丙三醇 |
| C | 若X、Y分子中分别有1个、2个碳原子 | Z的摩尔质量不小于60 g•mol-1 |
| D | 若X、Y均存在醇类同分异构体 | Z一定存在醇类同分异构体 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.只有连接醇羟基碳原子相邻碳原子上含有H原子的醇能发生消去反应;
B.乙醇和丙三醇结构不相似;
C.Y分子中2个碳原子,式量最小为乙醇,则Z为丙醇;
D.若X、Y均存在醇类同分异构体,Z不一定含有同分异构体.
解答 解:A.X、Y、Z 三种醇互为同系物,如丙醇、乙醇、甲醇,丙醇、乙醇能发生消去反应,甲醇CH3OH,-OH相连碳没有相邻碳,无法发生消去反应,故A错误;
B.乙醇含有1个醇羟基、丙三醇含有3个醇羟基,所以乙醇和丙三醇结构不相似,二者不是同系物,故B错误;
C.X、Y、Z 三种醇互为同系物,X、Y分子中分别含有1个、2个碳原子,Y分子中2个碳原子,式量最小为乙醇,则Z为丙醇,其摩尔质量等于60g.mol-1,若Y为乙二醇,则Z为丙二醇,摩尔质量大于60g.mol-1,故C正确;
D.X、Y、Z 三种醇互为同系物,如丁醇、戊醇、乙醇,乙醇不存在醇类同分异构体,故D错误;
故选C.
点评 本题考查有机物结构和性质,为高频考点,侧重考查学生分析判断能力,明确醇发生消去反应结构特点、同分异构体判断方法是解本题关键,采用举例法分析解答,题目难度中等.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
11.1mol丙醇与3mol乙酸在一定条件下反应生成乙酸乙酯和水,下列关于该反应的说法正确的是( )
| A. | 丙醇与乙酸的反应条件通常是浓硫酸、加热 | |
| B. | 充分反应可以生成1mol乙酸乙酯 | |
| C. | 生成的乙酸丙酯和水的物质的量之比是1:2 | |
| D. | 反应结束时,剩余2mol乙酸 |
1.绿矾(FeSO4•7H2O)是治疗缺铁性贫血药品的重要成分,也可用来制备多种铁的化合物.回答下列问题:
(1)实验室以绿矾为原料,通过以下过程制备磁性Fe3O4胶体粒子:
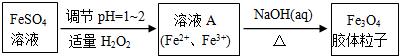
①写出FeSO4溶液转化为溶液A发生反应的离子方程式:2Fe2++H2O2+2H+═2Fe3++2H2O.
②Fe3O4胶体粒子不能用过滤法实现分离,理由是胶体粒子的直径较小(在10-7~10-9m),过滤时可透过滤纸.
③一定条件下,Fe3+水解生成聚合物的离子方程式为:xFe3++yH2O?Fex(OH)y(3x-y)++yH+
欲使平衡正向移动可采用的方法有abd(填字母).
a.加水稀释 b.加入少量NaCl溶液
c.降温 d.加入少量Na2CO3固体
④设计一个实验,证明溶液A中既含有Fe3+又含有Fe2+:取少量溶液A于洁净的试管中,加入硫氰化钾溶液,溶液显红色,说明溶液中含有Fe3+;另取少量溶液A于另一洁净的试管中,滴入酸性高锰酸钾溶液,振荡后溶液颜色从紫红色变成黄色说明溶液含有Fe2+.
(2)柠檬酸亚铁(FeC6H6O7)是一种易吸收的高效铁制剂,可由绿矾通过下列反应制备:
FeSO4+Na2CO3═FeCO3↓+Na2SO4 FeCO3+C6H8O7═FeC6H6O7+CO2↑+H2O
下表列出了Fe2+生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
①制备FeCO3时,将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中,目的是避免生成Fe(OH)2沉淀.
②将制得的FeCO3加入到足量柠檬酸溶液中,再加入少量铁粉,80℃下搅拌充分反应.反应结束后,无需过滤,再加入适量的柠檬酸溶液即可除去过量铁粉.该反应的化学方程式为Fe+C6H8O7=FeC6H6O7+H2↑.
③上述溶液经浓缩后,加入适量无水乙醇,静置、过滤、洗涤、干燥,得到柠檬酸亚铁晶体.分离过程中加入无水乙醇的目的是降低柠檬酸亚铁在水中的溶解量,有利于晶体析出.
(3)正常人每天应补充13.0mg左右的铁,如果全部通过服用含FeSO4•7H2O的片剂来补充铁,则正常人每天需服用含64.5mg FeSO4•7H2O的片剂(保留一位小数).
(1)实验室以绿矾为原料,通过以下过程制备磁性Fe3O4胶体粒子:
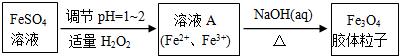
①写出FeSO4溶液转化为溶液A发生反应的离子方程式:2Fe2++H2O2+2H+═2Fe3++2H2O.
②Fe3O4胶体粒子不能用过滤法实现分离,理由是胶体粒子的直径较小(在10-7~10-9m),过滤时可透过滤纸.
③一定条件下,Fe3+水解生成聚合物的离子方程式为:xFe3++yH2O?Fex(OH)y(3x-y)++yH+
欲使平衡正向移动可采用的方法有abd(填字母).
a.加水稀释 b.加入少量NaCl溶液
c.降温 d.加入少量Na2CO3固体
④设计一个实验,证明溶液A中既含有Fe3+又含有Fe2+:取少量溶液A于洁净的试管中,加入硫氰化钾溶液,溶液显红色,说明溶液中含有Fe3+;另取少量溶液A于另一洁净的试管中,滴入酸性高锰酸钾溶液,振荡后溶液颜色从紫红色变成黄色说明溶液含有Fe2+.
(2)柠檬酸亚铁(FeC6H6O7)是一种易吸收的高效铁制剂,可由绿矾通过下列反应制备:
FeSO4+Na2CO3═FeCO3↓+Na2SO4 FeCO3+C6H8O7═FeC6H6O7+CO2↑+H2O
下表列出了Fe2+生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe2+ | 5.8 | 8.8 |
②将制得的FeCO3加入到足量柠檬酸溶液中,再加入少量铁粉,80℃下搅拌充分反应.反应结束后,无需过滤,再加入适量的柠檬酸溶液即可除去过量铁粉.该反应的化学方程式为Fe+C6H8O7=FeC6H6O7+H2↑.
③上述溶液经浓缩后,加入适量无水乙醇,静置、过滤、洗涤、干燥,得到柠檬酸亚铁晶体.分离过程中加入无水乙醇的目的是降低柠檬酸亚铁在水中的溶解量,有利于晶体析出.
(3)正常人每天应补充13.0mg左右的铁,如果全部通过服用含FeSO4•7H2O的片剂来补充铁,则正常人每天需服用含64.5mg FeSO4•7H2O的片剂(保留一位小数).
5.六氟化硫分子呈正八面体(如图所示),在高电压下仍有良好的绝缘性,性质稳定,在电器工业方面有着广泛的用途,但逸散到空气中会引起强温室效应,下列有关六氟化硫的推测正确的是( )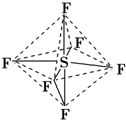

| A. | 六氟化硫中各原子均为8电子稳定结构 | |
| B. | 六氟化硫易燃烧生成二氧化硫 | |
| C. | 六氟化硫分子中含极性键、非极性键 | |
| D. | S-F键是σ键,且键长、键能都相等 |
15.你认为下列说法不正确的是( )
| A. | 氢键存在于分子之间,不存在于分子之内 | |
| B. | 对于组成和结构相似的分子,其范德华力随着相对分子质量的增大而增大 | |
| C. | NH3极易溶于水而CH4难溶于水的原因只是NH3是极性分子,CH4是非极性分子 | |
| D. | 冰熔化时只破坏分子间作用力 |
2. TiO2在光照射下可使水电解:2H2O$\frac{\underline{\;TiO_{2}\;}}{光}$在2H2↑+O2↑,该过程类似植物的光合作用.如图是光照射下TiO2分解水的装置示意图.下列叙述正确的是( )
TiO2在光照射下可使水电解:2H2O$\frac{\underline{\;TiO_{2}\;}}{光}$在2H2↑+O2↑,该过程类似植物的光合作用.如图是光照射下TiO2分解水的装置示意图.下列叙述正确的是( )
 TiO2在光照射下可使水电解:2H2O$\frac{\underline{\;TiO_{2}\;}}{光}$在2H2↑+O2↑,该过程类似植物的光合作用.如图是光照射下TiO2分解水的装置示意图.下列叙述正确的是( )
TiO2在光照射下可使水电解:2H2O$\frac{\underline{\;TiO_{2}\;}}{光}$在2H2↑+O2↑,该过程类似植物的光合作用.如图是光照射下TiO2分解水的装置示意图.下列叙述正确的是( )| A. | 该装置可以将光能转化为电能,同时也能转化为化学能 | |
| B. | 铂电极上发生的反应为:H2-2e-=2H+ | |
| C. | 该装置工作时,电流由TiO2电极经R流向铂电极 | |
| D. | 该装置工作时,TiO2电极附近溶液的pH变大 |
19.下列元素的原子半径依次增大的是( )
| A. | Na Mg Al | B. | Na O F | C. | P Si Al | D. | C Si P |
20.下列叙述正确的是( )
| A. | 随着核电荷数增加,碱金属单质的密度逐渐增大 | |
| B. | 随着核电荷数增加,卤素单质的熔沸点逐渐降低 | |
| C. | 随着核电荷数的增加,碱金属单质与水反应的剧烈程度增大 | |
| D. | 随着核电荷数增加,碱金属离子的氧化性逐渐增强,卤素离子的还原性逐渐减弱 |