题目内容
13.某K2CO3样品中含有Na2CO3、KNO3和Ba(NO3)2三种杂质中的一种或两种,现将6.9g样品溶于足量水中,得到澄清溶液,若再加入过量的CaCl2溶液,得到4.0g沉淀,对样品所含杂质的正确判断是( )| A. | 肯定有KNO3和Na2CO3,没有Ba(NO3)2 | |
| B. | 肯定有KNO3,没有Ba(NO3)2,可能还有Na2CO3 | |
| C. | 肯定没有Na2CO3和Ba(NO3)2,可能有KNO3 | |
| D. | 以上判断都不正确 |
分析 取样品加入水中,得到澄清溶液,则不可能含有Ba(NO3)2,因为碳酸钡不溶于水,再加入过量的CaCl2溶液能产生4.0g沉淀为碳酸钙的质量,假设6.9g全部为K2CO3,计算反应生成碳酸钙的质量,再结合生成沉淀的质量判断杂质中含有碳酸根的质量分数与K2CO3中碳酸根的质量分数大小.
解答 解:取样品加入水中,得到澄清溶液,则不可能含有Ba(NO3)2,因为碳酸钡不溶于水,再加入过量的CaCl2溶液能产生4.0g沉淀为碳酸钙的质量,假设6.9g全部为K2CO3,则生成沉淀为$\frac{6.9g}{138g/mol}$×100g/mol=5g>4.0g,则杂质中含有碳酸根的质量分数应小于K2CO3中碳酸根的质量分数,故一定有KNO3,可能还有Na2CO3,
故选:B.
点评 本题考查混合物反应的有关计算、物质推断等,题目难度中等,注意利用极限法确定杂质中碳酸根质量分数与碳酸钾中质量分数关系.

练习册系列答案
相关题目
13.在密闭容器中下列可逆反应达到平衡,增大压强和升高温度都能使平衡向正反应方向移动的是( )
| A. | N2(气体)+O2(气体)?2NO(气体) 正反应吸热 | |
| B. | NH4HCO3(固体)?NH3(气体)+H2O(气体)+CO2(气体) 正反应吸热 | |
| C. | 3O2(气体)?2O3(气体) 正反应吸热 | |
| D. | 2NO2(气体)?N2O4(气体) 正反应放热 |
1.常温下某溶液中由水电离产生的[H+]=1×10-5mol•L-1,则下列叙述正确的是( )
| A. | 一定是碱溶液 | B. | 一定是酸溶液 | ||
| C. | 由水电离出的[OH-]=1×10-9mol•L-1 | D. | pH值可能为9也可能为5 |
8.向含有1.2mol的FeCl2溶液中通入0.3molCl2,再加入含0.1mol X2O72- 的酸性溶液,使溶液中Fe2+全部恰好氧化,并使 X2O72- 还原为Xn+,则n值为( )
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
18.下列熔、沸点高低的比较不正确的是( )
| A. | 金刚石>碳化硅>晶体硅 | B. | 邻羟基苯甲酸>对羟基苯甲酸 | ||
| C. | 纯铁>生铁 | D. | MgO>MgCl2 |
5.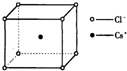 如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cs+离子核间距为a cm,氯化铯的摩尔质量为M,则氯化铯晶体的密度为d g•cm-3,阿伏加德罗常数的值可表示为( )
如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cs+离子核间距为a cm,氯化铯的摩尔质量为M,则氯化铯晶体的密度为d g•cm-3,阿伏加德罗常数的值可表示为( )
 如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cs+离子核间距为a cm,氯化铯的摩尔质量为M,则氯化铯晶体的密度为d g•cm-3,阿伏加德罗常数的值可表示为( )
如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cs+离子核间距为a cm,氯化铯的摩尔质量为M,则氯化铯晶体的密度为d g•cm-3,阿伏加德罗常数的值可表示为( )| A. | 2Ma3d | B. | M/(a3d) | C. | M/(2a3d) | D. | 2M/(a3d) |
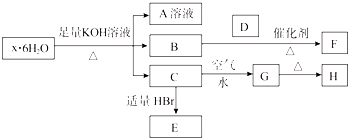
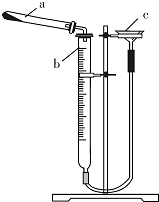 碱式碳酸铜是一种具有广泛用途的化工产品,主要用于固体荧光粉激活剂和铜盐的制造等.
碱式碳酸铜是一种具有广泛用途的化工产品,主要用于固体荧光粉激活剂和铜盐的制造等.