题目内容
6.某溶液由K+、Cu2+、Ba2+、Fe3+、CO32-、SO42-、Cl-中的若干种离子组成,取适量该溶液进行如下实验:①向其中加入过量盐酸,有气体生成,并得到无色透明溶液;
②在①所得溶液中加入过量氢氧化钡溶液,产生白色沉淀,过滤;
③在②所得的滤液中加入过量稀硝酸,再加入硝酸银溶液,产生白色沉淀.
根据上述实验回答下列问题:
(1)原溶液中一定不存在的离子是Cu2+、Ba2+、Fe3+;
(2)原溶液中一定存在的离子是CO32-、SO42-、K+;
(3)原溶液中可能存在的离子是Cl-,请解释不能确定离子是否存在的原因:由于在①中加入了过量的盐酸,盐酸电离出的Cl-与Ag+反应生成氯化银白色沉淀,因而无法确定原溶液中是否含有Cl-.
分析 ①向其中加入过量盐酸,有气体生成,并得到无色透明溶液,则一定不含有色离子Cu2+、Fe3+,一定含弱酸根离子CO32-,则不含Ba2+;
②在①所得溶液中加入过量氢氧化钡溶液,产生白色沉淀,过滤,白色沉淀为硫酸钡,则一定含SO42-;
③在②所得的滤液中加入过量稀硝酸,再加入硝酸银溶液,产生白色沉淀,白色沉淀为AgCl,①中加盐酸引入氯离子,则不一定含Cl-,以此来解答.
解答 解:①向其中加入过量盐酸,有气体生成,并得到无色透明溶液,则一定不含有色离子Cu2+、Fe3+,一定含弱酸根离子CO32-,则不含Ba2+;
②在①所得溶液中加入过量氢氧化钡溶液,产生白色沉淀,过滤,白色沉淀为硫酸钡,则一定含SO42-;
③在②所得的滤液中加入过量稀硝酸,再加入硝酸银溶液,产生白色沉淀,白色沉淀为AgCl,①中加盐酸引入氯离子,则不一定含Cl-,
由电荷守恒可知,一定含阳离子为K+,
(1)由上述分析可知,一定不存在Cu2+、Ba2+、Fe3+,故答案为:Cu2+、Ba2+、Fe3+;
(2)原溶液中一定存在的离子是CO32-、SO42-、K+,故答案为:CO32-、SO42-、K+;
(3)原溶液中可能存在的离子是Cl-;由于在①中加入了过量的盐酸,盐酸电离出的Cl-与Ag+反应生成氯化银白色沉淀,因而无法确定原溶液中是否含有Cl-,
故答案为:Cl-;由于在①中加入了过量的盐酸,盐酸电离出的Cl-与Ag+反应生成氯化银白色沉淀,因而无法确定原溶液中是否含有Cl-.
点评 本题考查常见离子的推断,为高频考点,把握离子的颜色、离子之间的反应及现象为解答的关键,侧重分析与推断能力的考查,注意氯离子的推断为解答的易错点,题目难度不大.

练习册系列答案
相关题目
17.下列说法中正确的是( )
| A. | 需要加热才能发生的反应一定是吸热反应,吸热反应的生成物总能量一定高于反应物总能量 | |
| B. | 同温同压下,H2(g)+Cl2(g)═2HCl(g) 在光照和点燃条件下的△H不同 | |
| C. | 一定条件下,0.5 mol N2和1.5 mol H2置于某密闭容器中充分反应生成NH3气,放热19.3kJ,其热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ/mol | |
| D. | 一定条件下4 HCl(g)+O2(g)═2Cl2(g)+2H2O(g),当1 mol O2反应放出115.6 kJ热量,键能如下所示,则断裂1 mol H-O键与断裂1 mol H-Cl键所需能量差为31.9 kJ Cl2(g)$\stackrel{243kJ/mol}{→}$2Cl(g) O2(g)$\stackrel{498kJ/mol}{→}$2O(g) |
1.下列仪器用于过滤和蒸发分离物质的是( )
①漏斗 ②试管 ③蒸发皿 ④天平 ⑤烧杯 ⑥研钵.
①漏斗 ②试管 ③蒸发皿 ④天平 ⑤烧杯 ⑥研钵.
| A. | ①③④ | B. | ①②⑥ | C. | ①③⑤ | D. | ①③⑥ |
15.常温下,pH值相同的三种盐NaX、NaY和NaZ的溶液,其物质的量浓度为NaX>NaY>NaZ.下列说法正确的是( )
| A. | 三种酸的酸性为HX<HY<HZ | |
| B. | 物质的量浓度相同的三种盐的水溶液中,NaZ的溶液中,水的电离程度最大 | |
| C. | pH值相同的三种酸的水溶液,恰好中和时所耗NaOH的物质的量为HX<HY<HZ | |
| D. | 物质的量浓度相同的HZ和NaX能发生HZ+NaX=HX+NaZ |
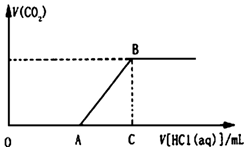 向100mL某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2,使其充分反应.在上述所得溶液中,逐滴缓慢滴加1mol•L-1的盐酸,所得气体(不考虑溶解)的体积与滴加盐酸的体积关系如图(其中点A是线段OC上的动点):
向100mL某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2,使其充分反应.在上述所得溶液中,逐滴缓慢滴加1mol•L-1的盐酸,所得气体(不考虑溶解)的体积与滴加盐酸的体积关系如图(其中点A是线段OC上的动点):
 CH3COOCH2CH3+H2O;反应类型酯化反应.
CH3COOCH2CH3+H2O;反应类型酯化反应.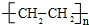 ;反应类型加聚反应.
;反应类型加聚反应.