题目内容
下列说法正确的是( )
| A、有些活泼金属如铝可作还原法的还原剂 |
| B、用电解氯化钠溶液的方法可冶炼金属钠 |
| C、可用焦炭或一氧化碳还原氧化铝的方法来冶炼铝 |
| D、利用太阳能,无法将海水蒸馏淡化 |
考点:氧化还原反应,反应热和焓变,金属冶炼的一般原理
专题:
分析:金属的活泼性不同,冶炼方法不同,K、Ca、Na、Mg、Al等金属可用电解法冶炼,Zn、Fe、Sn、Pb、Cu、Hg等金属可用热还原法冶炼,Ag、Hg等金属可用热分解法冶炼,热还原法的还原剂可用C、CO等,如冶炼温度较高,可用Al为还原剂,以此解答该题.
解答:
解:A.Al具有较强的还原性,Al可用于铝热反应的还原剂,可用于冶炼铁等金属,用于焊接钢轨,故A正确;
B.冶炼金属钠,应用电解熔融的氯化钠的方法,电解氯化钠溶液得到氢氧化钠、氢气和氯气,故B错误;
C.铝为活泼金属,应用电解熔融的氧化铝的方法冶炼,故C错误;
D.利用太阳能可以使海水挥发,则利用太阳能,能将海水蒸馏淡化,故D错误.
故选A.
B.冶炼金属钠,应用电解熔融的氯化钠的方法,电解氯化钠溶液得到氢氧化钠、氢气和氯气,故B错误;
C.铝为活泼金属,应用电解熔融的氧化铝的方法冶炼,故C错误;
D.利用太阳能可以使海水挥发,则利用太阳能,能将海水蒸馏淡化,故D错误.
故选A.
点评:本题考查金属的冶炼,侧重于基础知识的考查,注意把握金属的冶炼方法和金属活泼性之间的关系,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列各组离子在溶液中能大量共存的是( )
| A、Ba2+,Cl-,SO42-,K+ |
| B、K+,H+,CO32-,Na+ |
| C、Mg2+,Cl-,SO42-,K+ |
| D、Ag+,NO3-,Cl-,K+ |
厨房中的化学知识很多,下面是有关厨房中的常见操作或者常见现象,其中属于氧化还原反应的是( )
| A、食醋不慎洒落到大理石台面出现腐蚀现象 |
| B、做馒头用的发面中常加入少许碱面(小苏打)揉和 |
| C、烧菜用过的铁锅,经放置常出现红棕色斑迹 |
| D、粗盐潮解 |
能正确表示下列反应的离子方程式的是( )
| A、用CH3COOH溶解CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑ |
| B、将过量的SO2通入Ca(ClO)2溶液中:SO2+ClO-+H2O=HClO+HSO3- |
| C、硫酸亚铁溶液中加入酸化的双氧水:2Fe2++2H++H2O2=2Fe3++2H2O |
| D、等物质的量的MgC12、Ba(OH)2和HCl溶液混合:Mg2++2OH-=Mg( OH)2↓ |
下列事实不能用勒夏特列原理解释的是( )
| A、溴水中有下列平衡Br2+H2O?HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅 |
| B、加催化剂,使N2和H2在一定条件下转化为NH3 |
| C、反应CO(g)+NO2(g)═CO2(g)+NO(g)△H<0,达平衡后,升高温度体系颜色变深 |
| D、增大压强,有利于SO2与O2反应生成SO3 |
下列化学用语正确的是( )
A、NaCl的电子式: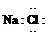 |
| B、乙醇的结构简式:C2H6O |
C、Mg原子结构示意图: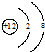 |
| D、乙酸乙酯的分子式:C4H8O2 |