题目内容
18.在一定体积的容器中,加入1.5mol氙气(Xe)和7.5mol氟气(F2),于400℃和2633kPa下加热数小时,然后迅速冷却至25℃,容器内除得到一种无色晶体外,还余下4.5molF2.推算该无色晶体的化学式.分析 开始加入1.5mol氙气和7.5mol氟气,剩余4.5mol氟气,完全反应氙气,参加反应氟气为3mol,根据质量守恒定律确定晶体的化学式.
解答 解:开始加入1.5mol氙气和7.5mol氟气,剩余4.5mol氟气,完全反应氙气,参加反应的氟气为7.5mol-4.5mol=3mol,1.5molXe与3moL氟气反应生成物中Xe原子与氟原子物质的量之比为1.5:3×2=1:4,所以化学式为:XeF4,答:该无色晶体的化学式为XeF4.
点评 本题考查化学方程式计算,涉及质量守恒定律,明确反应前后同种元素原子数目不变即可解答.

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
8.下列试剂长期敞放空气中,不会发生化学变化的是( )
| A. | 氯水 | B. | 氧化钠 | C. | 漂白粉 | D. | 氯化钙 |
9.中新网2013年5月3日报道,${\;}_{26}^{60}$Fe的现身揭秘了超新星爆炸历史真相.下列说法中正确的是( )
| A. | 铁原子的质量数均为60 | |
| B. | ${\;}_{26}^{60}$Fe的核内质子数比中子数多8 | |
| C. | 1mol${\;}_{26}^{58}$Fe与足量盐酸反应时均可得到1mol H2 | |
| D. | 等物质的量的${\;}_{26}^{60}$Fe与1mol ${\;}_{26}^{58}$Fe,前者质量比后者多2g |
6.下列对化学反应的认识不正确的是( )
| A. | 会引起化学键的变化 | B. | 必然引起物质状态的变化 | ||
| C. | 必然伴随着能量的变化 | D. | 会产生新的物质 |
13.相同温度、相同浓度下的六种盐溶液,其pH由小到大的顺序如图所示,图中①②③代表的物质可能分别为( )


| A. | CH3COOH HCl CH3COONa | B. | H2SO4 (NH4)2SO4 CH3COONa | ||
| C. | (NH4)2SO4 CH3COOH NaOH | D. | (NH4)2SO4 NH4Cl CH3COONa |
10.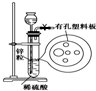 如图为实验室制氢气的简易装置.若在加稀硫酸时发现锌粒与稀硫酸没有接触而稀硫酸不够了,为使该反应顺利进行,可以从长颈漏斗中加入的试剂是( )
如图为实验室制氢气的简易装置.若在加稀硫酸时发现锌粒与稀硫酸没有接触而稀硫酸不够了,为使该反应顺利进行,可以从长颈漏斗中加入的试剂是( )
①食盐水
②KNO3溶液
③适量稀硫酸铜溶液
④Na2CO3溶液
⑤CCl4
⑥浓氨水.
 如图为实验室制氢气的简易装置.若在加稀硫酸时发现锌粒与稀硫酸没有接触而稀硫酸不够了,为使该反应顺利进行,可以从长颈漏斗中加入的试剂是( )
如图为实验室制氢气的简易装置.若在加稀硫酸时发现锌粒与稀硫酸没有接触而稀硫酸不够了,为使该反应顺利进行,可以从长颈漏斗中加入的试剂是( )①食盐水
②KNO3溶液
③适量稀硫酸铜溶液
④Na2CO3溶液
⑤CCl4
⑥浓氨水.
| A. | ①③⑤ | B. | ①②③ | C. | ④⑤⑥ | D. | ①②③⑤ |
5.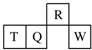 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )| A. | 最简单气态氢化物的热稳定性:R>Q | |
| B. | 最高价氧化物对应水化物的酸性:Q<W | |
| C. | 原子半径:T>Q>R | |
| D. | T的非金属性强于Q的非金属性 |
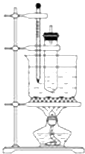 苯与浓硝酸的反应:实验室制备硝基苯的实验装置如下图所示,主要步骤如下:
苯与浓硝酸的反应:实验室制备硝基苯的实验装置如下图所示,主要步骤如下: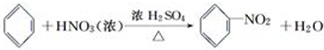 .
.