题目内容
2.下列气态氢化物中最稳定的是( )| A. | H2O | B. | PH3 | C. | HF | D. | NH3 |
分析 根据元素非金属性越强,氢化物的稳定性越强来判断,同周期从左到右元素的非金属性增强,同主族从上到下非金属性减弱.
解答 解:对于P、N、O、F四种非金属元素来说,N、O、F处于同一周期,同周期从左到右元素的非金属性增强,即非金属性N<O<F;
N和P处于同一主族,同主族从上到下非金属性减弱,即非金属性N>P.
因此,非金属性最强的是F元素,元素非金属性越强,氢化物的稳定性越强,则氢化物最稳定的是HF.
故选C.
点评 本题考查了元素周期律,侧重于非金属性和氢化物的稳定性比较的考查,题目难度不大,注意把握同主族和同周期元素性质的变化规律.

练习册系列答案
相关题目
15.不锈钢表面用硝酸和氢氟酸的混酸处理后,产生的酸洗废液中含有Fe3+、Ni2+、NO3-、F-和+6价铬的含氧酸根离子等.如图是综合利用该酸洗废液的工艺流程:
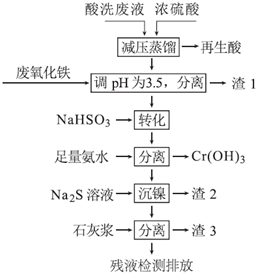
已知:
①金属离子开始沉淀和沉淀完全时的pH:
②Ni2+与足量氨水的反应为:Ni2++6NH3?[Ni(NH3)6]2+
(1)再生酸中含有硝酸、氢氟酸,采取减压蒸馏的原因是降低蒸馏的温度以减少硝酸的分解.
(2)利用废氧化铁(主要成分为Fe2O3)代替烧碱调节pH的好处是实现废物利用,降低生产成本.
(3)请写出“转化”时NaHSO3与Cr2O72-发生反应的离子反应方程式:Cr2O72-+3HSO3-+5H+=2Cr3++3SO42-+4H2O.
(4)已知[Ni(NH3)6]2+为难电离的络合离子,则“沉镍”的离子方程式为:[Ni(NH3)6]2++S2-=NiS↓+6NH3.
(5)滤渣3的主要成分为CaF2、Ca(OH)2和CaSO4.
(6)经检测,最后的残液中c(Ca2+)=0.004mol•L-1,则残液中F-浓度为1.9mg•L-1,符合(填“符合”或“不符合”)排放标准[已知Ksp(CaF2)=4×10-11 mol3•L-3,国家排放标准要求氟离子浓度小于10mg•L-1].

已知:
①金属离子开始沉淀和沉淀完全时的pH:
| Fe3+ | Ni2+ | Cr3+ | |
| 开始沉淀 | 1.5 | 6.7 | 4.0 |
| 沉淀完全 | 3.4 | 9.5 | 6.9 |
(1)再生酸中含有硝酸、氢氟酸,采取减压蒸馏的原因是降低蒸馏的温度以减少硝酸的分解.
(2)利用废氧化铁(主要成分为Fe2O3)代替烧碱调节pH的好处是实现废物利用,降低生产成本.
(3)请写出“转化”时NaHSO3与Cr2O72-发生反应的离子反应方程式:Cr2O72-+3HSO3-+5H+=2Cr3++3SO42-+4H2O.
(4)已知[Ni(NH3)6]2+为难电离的络合离子,则“沉镍”的离子方程式为:[Ni(NH3)6]2++S2-=NiS↓+6NH3.
(5)滤渣3的主要成分为CaF2、Ca(OH)2和CaSO4.
(6)经检测,最后的残液中c(Ca2+)=0.004mol•L-1,则残液中F-浓度为1.9mg•L-1,符合(填“符合”或“不符合”)排放标准[已知Ksp(CaF2)=4×10-11 mol3•L-3,国家排放标准要求氟离子浓度小于10mg•L-1].
13.图中a、b、c、d、e、f表示元素周期表中部分短周期元素,下列叙述正确的是( )


| A. | a、b、c的简单离子中,b的离子半径最大 | |
| B. | c、d、f最高价氧化物对应的水化物两两之间均可发生反应 | |
| C. | e的氢化物比f的氢化物的稳定性高 | |
| D. | 离子半径a3-小于d3+ |
10.最近,中国科大的科学家们将C60分子组装在一单层分子膜表面,在-268℃时冻结分子的热振荡,并利用扫描隧道显微镜首次“拍摄”到能清楚分辨碳原子间单、双键的分子图象.下列化合物分子中一定既含σ键又含π键的是( )
| A. | CO2 | B. | COCl2 | C. | C2H6O | D. | H2O2 |
17.下列关于有机物的正确说法是( )
| A. | 聚乙烯可发生加成反应 | B. | 石油干馏可得到汽油、煤油等 | ||
| C. | 苯不能发生氧化反应 | D. | 甲苯能被高锰酸钾氧化 |
7.下列各化合物中,能发生酯化、还原、加成、消去四种反应的是( )
| A. | 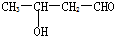 | B. |  | C. | CH3-CH=CH-CHO | D. | 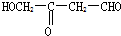 |
14.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,22.4LH2的分子数为1NA | |
| B. | 0 5mol•L-1的MgCl2溶液,含有Cl数为1NA | |
| C. | 56g铁片投人足量的浓硫酸中生成1.5NA个SO2分子 | |
| D. | 常温常压下,14gN2含有分子数为0.5NA |
11.氯气和漂白粉是现代工业和生活中常用的消毒液、杀菌剂.
(1)写出工业上用氯气和石灰乳制取漂白粉的化学方程式2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O
(2)实验室有一瓶密封不严的漂白粉样品,其中一定含有CaCl2、Ca(OH)2,请设计实验,探究该样品中可能存在的其它固体物质
①提出合理假设
假设1:该漂白粉未变质,含Ca(ClO)2
假设2:该漂白粉全部变质,含CaCO3
假设3:该漂白粉部分变质,则含有CaCO3和Ca(ClO)3
②设计实验方案,进行实验,并完成实验报告.
(1)写出工业上用氯气和石灰乳制取漂白粉的化学方程式2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O
(2)实验室有一瓶密封不严的漂白粉样品,其中一定含有CaCl2、Ca(OH)2,请设计实验,探究该样品中可能存在的其它固体物质
①提出合理假设
假设1:该漂白粉未变质,含Ca(ClO)2
假设2:该漂白粉全部变质,含CaCO3
假设3:该漂白粉部分变质,则含有CaCO3和Ca(ClO)3
②设计实验方案,进行实验,并完成实验报告.
| 实验步骤 | 预期现象和结论 | |
| ① | 取样品于试管中,加入适量2.0mol•L-1盐酸溶解后,再将产生的气体经蒸馏水、四氯化碳后导入澄清石灰水中 | a.若澄清石灰水未见浑浊,则假设1成立 b.若澄清石灰水变浑浊,则假设2或3成立 |
| ② | 取样品于试管中,加入适量2.0mol•L-1盐酸溶解后,再向试管中滴入1-2滴品红溶液,振荡 | 若品红褪色,结合实验①中的现象和结论b,则假设3 成立 |