题目内容
下列分子中所有的原子最外层达到8电子构型的是( )
| A、BF3 |
| B、SiH4 |
| C、SF6 |
| D、PCl3 |
考点:原子核外电子排布
专题:原子组成与结构专题
分析:分子中原子的最外层电子数可以根据每种元素原子的最外层电子数与化合价的绝对值之和来判断.含有H元素的化合物一定不能所有原子达到8的稳定结构.
解答:
解:A.BF3中,B最外层电子数,则3+3≠8,不满足分子中所有原子都满足最外层8电子结构,故A错误;
B.SiH4含有H元素,h达到2个电子的稳定结构,所以该分子中所有原子不能都达到8电子稳定结构,故B错误;
C.SF6中S的最外层电子数为6,化合价为+6,6+6=10,所以该分子中一定不是所有原子达到8电子稳定结构,故C错误;
D.PCl3中,P的价电子数为5,化合价为+3价,C的最外层数为5+3=8,满足8电子稳定结构,Cl的价电子数为7,化合价为-1价,Cl的最外层电子数为7+|-1|=8,满足8电子稳定结构,故D正确;
故选D.
B.SiH4含有H元素,h达到2个电子的稳定结构,所以该分子中所有原子不能都达到8电子稳定结构,故B错误;
C.SF6中S的最外层电子数为6,化合价为+6,6+6=10,所以该分子中一定不是所有原子达到8电子稳定结构,故C错误;
D.PCl3中,P的价电子数为5,化合价为+3价,C的最外层数为5+3=8,满足8电子稳定结构,Cl的价电子数为7,化合价为-1价,Cl的最外层电子数为7+|-1|=8,满足8电子稳定结构,故D正确;
故选D.
点评:本题考查了8电子稳定结构的判断,根据中心原子族序数与成键个数的和判断即可,还可以根据中心原子价电子数与配原子个数判断,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
将下列各种单质投入或通入CuSO4溶液中,能产生铜单质的是( )
| A、Fe | B、Na |
| C、H2 | D、Ag |
一定温度下,在2L的密闭容器中加入4molA和6molB,发生如下反应:2A(g)+3B(g)?4C(g)+D(g)反应10min后达平衡,此时D的浓度为0.5mol/L.下列说法正确的是( )
| A、前10min反应的平均速率V(C)=0.10mol/L?min |
| B、10min后向容器中加入A,重新平衡时A的转化率一定大于50% |
| C、恒温下将反应容器体积缩小一半,则D的平衡浓度小于1.0mol/L |
| D、反应达平衡时B的平衡浓度是1.5mol/L |
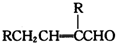
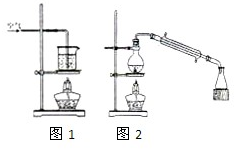 某化学研究小组拟采用铜粉在酸溶液中直接通入空气氧化制备硫酸铜晶体.
某化学研究小组拟采用铜粉在酸溶液中直接通入空气氧化制备硫酸铜晶体.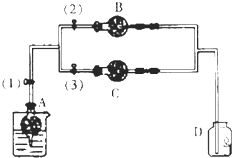 在干燥管A中的块状白色固体为某种正盐,B中为淡黄色粉末,C中为白色粉末,并将A、B、C按图所示连接.打开活塞(1)(3)时,D中蜡烛火焰熄灭,C中白色粉末变蓝;当打开活塞(1)(2)时,D中蜡烛火焰变得更明亮;关闭活塞(1)时,A中反应可自行停止.
在干燥管A中的块状白色固体为某种正盐,B中为淡黄色粉末,C中为白色粉末,并将A、B、C按图所示连接.打开活塞(1)(3)时,D中蜡烛火焰熄灭,C中白色粉末变蓝;当打开活塞(1)(2)时,D中蜡烛火焰变得更明亮;关闭活塞(1)时,A中反应可自行停止.