题目内容
13.下列关于铝的性质和用途描述正确的是( )| A. | 铝能与所有的酸和碱反应放出氢气 | |
| B. | 用酒精灯外焰加热铝箔,可以看到少量液滴悬而不落,说明铝的熔点比氧化铝高 | |
| C. | 铝合金质轻,强度大,耐腐蚀,可以用作门窗 | |
| D. | 氢氧化铝能溶于氨水 |
分析 A.铝与弱碱不发生反应;
B.少量液滴悬而不落,说明生成的氧化铝的熔点较高,三氧化二铝在铝的表面,所以加热铝箔的时候铝熔化了但是不会滴落;
C.铝合金具有质量轻,强度大,抗腐蚀能力比较强的优点;
D.氨水为弱碱,氢氧化铝不溶于氨水.
解答 解:A.铝与酸或强碱溶液反应生成氢气,而与氨水不发生反应,故A错误;
B.将铝箔用坩埚钳夹住放在酒精灯火焰上加热,铝和氧气反应生成了氧化铝,又因三氧化二铝的熔点高于铝的熔点,而三氧化二铝在铝的表面,所以加热铝箔的时候铝熔化了但是不会滴落,故B错误;
C.铝常温下能与空气中氧气反应,生成一层致密的氧化物保护膜,从而具有抗腐蚀性,铝合金材料的密度小,用以减轻列车质量,铝合金强度大,所以可用作门窗,故C正确;
D.氢氧化铝溶于强碱,不溶于弱碱,所以氢氧化铝不能溶于氨水,故D错误;
故选C.
点评 本题考查了铝的化学性质,题目难度不大,明确常见元素及其化合物性质为解答关键,注意铝能够溶于强碱溶液,不与氨水反应,试题侧重基础知识的考查,有利于培养学生的灵活应用能力.

练习册系列答案
相关题目
1.某金属首饰可能含有铜或银,欲检验其是否用纯金制成,可把样品浸入某溶液一段时间后,取出洗净、干燥后称量,根据质量是否变化即可判断.可以选用的溶液是( )
| A. | 稀硫酸 | B. | 盐酸溶液 | C. | 稀硝酸 | D. | 氢氧化钠溶液 |
8.和OH-具有相同质子数和不同电子数的微粒是( )
| A. | F | B. | Cl- | C. | NH3 | D. | NH2- |
2.已知:Fe2+能被稀硝酸氧化,反应方程式为:3Fe(NO3)2+4HNO3(稀)→3Fe(NO3)3+NO↑+2H2O
现将一定量的铁和铜的混合物分为等质量的4份,分别加入等浓度不同体积的质量分数为0.20的稀硝酸(假设反应中稀硝酸的还原产物只有NO),产生气体的体积(标准状况下)与剩余固体的质量如下表:
(1)由NO与HNO3的关系可知,稀硝酸的物质的量浓度为4 mol•L-1.
(2)稀硝酸的密度为1.26g/cm3.
(3)放出2240mL气体时,反应的离子方程式是3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O,放出4480mL气体时,消耗金属的质量为16.8g.
(4)原混合物中铁和铜的物质的量比为2:1.
(5)加入400mL稀硝酸,反应完全后,溶液中NO3-的物质的量为1.2mol.
(6)当溶液中Cu2+、Fe2+的物质的量浓度相等时,放出气体的体积7840mL(标准状况下).
现将一定量的铁和铜的混合物分为等质量的4份,分别加入等浓度不同体积的质量分数为0.20的稀硝酸(假设反应中稀硝酸的还原产物只有NO),产生气体的体积(标准状况下)与剩余固体的质量如下表:
| 硝酸体积(mL) | 100 | 200 | 300 | 400 |
| 剩余固体(g) | 18.0 | 9.6 | 0 | 0 |
| 放出气体的体积(mL) | 2240 | 4480 | 6720 |
(2)稀硝酸的密度为1.26g/cm3.
(3)放出2240mL气体时,反应的离子方程式是3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O,放出4480mL气体时,消耗金属的质量为16.8g.
(4)原混合物中铁和铜的物质的量比为2:1.
(5)加入400mL稀硝酸,反应完全后,溶液中NO3-的物质的量为1.2mol.
(6)当溶液中Cu2+、Fe2+的物质的量浓度相等时,放出气体的体积7840mL(标准状况下).
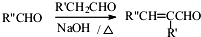
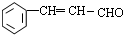 .
.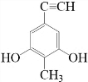 (或
(或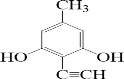 、
、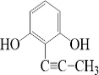 、
、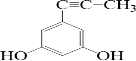 );.(任写一种)
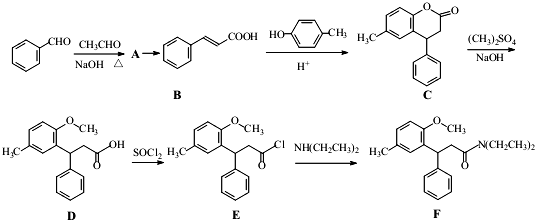
);.(任写一种)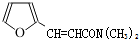 )是一种高效麻醉剂,写出以
)是一种高效麻醉剂,写出以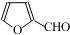 、CH3CHO、NH(CH3)2为原料制备呋喃丙胺的合成路线流程图(无机试剂自选).合成路线流程图示例如下:H2C=CH2$\stackrel{HBr}{→}$CHCH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.
、CH3CHO、NH(CH3)2为原料制备呋喃丙胺的合成路线流程图(无机试剂自选).合成路线流程图示例如下:H2C=CH2$\stackrel{HBr}{→}$CHCH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.