题目内容
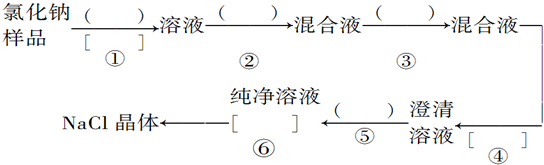
1.氯化钠样品含有少量的Na2SO4和Na2CO3,按下列流程进行净化.(1)请在流程图中的 ( )中写上合适的试剂,在[]中写上实验操作名称.
(2)写出有关反应的化学方程式:
第②步Na2SO4+BaCl2═BaSO4↓+2NaCl,Na2CO3+BaCl2═BaCO3↓+2NaCl;
第⑤步Na2CO3+2HCl═2NaCl+H2O+CO2↑.
分析 由流程可知,氯化钠样品含有少量的Na2SO4和Na2CO3,最后得到NaCl晶体,则①中加蒸馏水溶解,②中加BaCl2溶液,③加Na2CO3溶液,④为过滤得到澄清溶液,⑤中加稀盐酸,⑥为蒸发结晶,以此来解答.
解答 解:由流程可知,氯化钠样品含有少量的Na2SO4和Na2CO3,最后得到NaCl晶体,则①中加蒸馏水溶解,②中加BaCl2溶液,③加Na2CO3溶液,④为过滤得到澄清溶液,⑤中加稀盐酸,⑥为蒸发结晶,
(1)由上述分析可知,流程为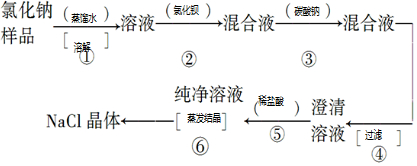 ,
,
故答案为:蒸馏水;溶解;BaCl2溶液;Na2CO3溶液;过滤;稀盐酸; 蒸发结晶;
(2)第②步中发生Na2SO4+BaCl2═BaSO4↓+2NaCl、Na2CO3+BaCl2═BaCO3↓+2NaCl,第⑤步发生Na2CO3+2HCl═2NaCl+H2O+CO2↑,
故答案为:Na2SO4+BaCl2═BaSO4↓+2NaCl;Na2CO3+BaCl2═BaCO3↓+2NaCl;Na2CO3+2HCl═2NaCl+H2O+CO2↑.
点评 本题考查混合物分离提纯,为高频考点,把握流程中的反应、混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意碳酸钠一定在氯化钡之后,题目难度不大.

练习册系列答案
相关题目
11.以下说法正确的是( )
| A. | mg的CO和H2混合气体充分燃烧后,生成的气体通入Na2O2固体中,固体质量增重mg | |
| B. | 将一定量的CO2气体通入足量的Na2O2固体中,固体量增重2.8g,则反应中有0.1mol电子转移 | |
| C. | 相同质量的铝分别与足量的盐酸和NaOH溶液反应,生成气体物质的量之比为1:3 | |
| D. | NaAlO2溶液中逐滴滴入盐酸至过量,生成的沉淀随着加入的元素所发生的变化如图所示: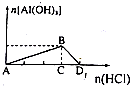 |
6.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 常温常压下,8 g CH4含有4NA个氢原子 | |
| B. | 2gD216O中含有的质子数为2NA个 | |
| C. | 1 mol Cu与足量FeCl3溶液反应,转移2NA个电子 | |
| D. | 通常状况下,2.24 L氮气含有0.1NA个N2分子 |
8.TiO2和TiCl4都是钛的重要化合物,某化学兴趣小组在实验室对两者的制备及性质进行探究.
Ⅰ.制备TiCl4
实验室利用反应TiO2 (s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,装置图和有关信息如下:

请回答下列问题:
(1)仪器A的名称是球形干燥管.
(2)实验开始前后的操作包括:①检查装置气密性,②组装仪器,③通N2一段时间,④加装药品,⑤点燃酒精灯⑥停止通N2⑦停止加热.正确的操作顺序是②①④③⑤⑦⑥
实验结束后欲分离D中的液态混合物,所采用操作的名称是蒸馏(或分馏).
(3)装置E能否不能(填“能”或“不能”)换成装置A,理由是装置A不能吸收空气中的氧气,不能保证反应在无氧环境下进行
(4)TiCl4是制取航天航空工业材料--钛合金的重要原料.某钛合金的元素还有Al和Si等,已知在常温下,钛是一种耐强酸强碱的金属,请设计实验检验其中的Si元素.
取少量合金样品于试管中,滴加过量NaOH溶液,振荡,静置后取上层清液,再逐滴滴入稀盐酸至过量,若有沉淀产生且最终沉淀不完全溶解,则证明样品中有Si
Ⅱ.制备TiO2及测定TiO2的质量分数:
在TiCl4中加水、加热,水解得到沉淀TiO2•xH2O,经过滤、水洗,再烘干、焙烧除去水分得到粉体TiO2.
(5)写出生成TiO2•xH2O的化学方程式TiCl4+(x+2)H2O$\frac{\underline{\;\;△\;\;}}{\;}$TiO2•xH2O↓+4HCl.
(6)检验沉淀是否洗涤干净的方法是取最后一次洗涤液于试管中加入硝酸酸化的AgNO3若没有产生沉淀,则已洗干净.
(7)一定条件下,将TiO2溶解并还原为Ti3+,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+.滴定分析时,称取上述TiO2试样0.2g,消耗0.1mol•L-1 NH4Fe(SO4)2标准溶液20mL
①配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的目的是:抑制NH4Fe(SO4)2水解.
②该滴定操作所用到的指示剂是KSCN溶液.
③则TiO2质量分数为80%.
Ⅰ.制备TiCl4
实验室利用反应TiO2 (s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,装置图和有关信息如下:

| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
(1)仪器A的名称是球形干燥管.
(2)实验开始前后的操作包括:①检查装置气密性,②组装仪器,③通N2一段时间,④加装药品,⑤点燃酒精灯⑥停止通N2⑦停止加热.正确的操作顺序是②①④③⑤⑦⑥
实验结束后欲分离D中的液态混合物,所采用操作的名称是蒸馏(或分馏).
(3)装置E能否不能(填“能”或“不能”)换成装置A,理由是装置A不能吸收空气中的氧气,不能保证反应在无氧环境下进行
(4)TiCl4是制取航天航空工业材料--钛合金的重要原料.某钛合金的元素还有Al和Si等,已知在常温下,钛是一种耐强酸强碱的金属,请设计实验检验其中的Si元素.
取少量合金样品于试管中,滴加过量NaOH溶液,振荡,静置后取上层清液,再逐滴滴入稀盐酸至过量,若有沉淀产生且最终沉淀不完全溶解,则证明样品中有Si
Ⅱ.制备TiO2及测定TiO2的质量分数:
在TiCl4中加水、加热,水解得到沉淀TiO2•xH2O,经过滤、水洗,再烘干、焙烧除去水分得到粉体TiO2.
(5)写出生成TiO2•xH2O的化学方程式TiCl4+(x+2)H2O$\frac{\underline{\;\;△\;\;}}{\;}$TiO2•xH2O↓+4HCl.
(6)检验沉淀是否洗涤干净的方法是取最后一次洗涤液于试管中加入硝酸酸化的AgNO3若没有产生沉淀,则已洗干净.
(7)一定条件下,将TiO2溶解并还原为Ti3+,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+.滴定分析时,称取上述TiO2试样0.2g,消耗0.1mol•L-1 NH4Fe(SO4)2标准溶液20mL
①配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的目的是:抑制NH4Fe(SO4)2水解.
②该滴定操作所用到的指示剂是KSCN溶液.
③则TiO2质量分数为80%.
9.生活垃圾无害化处理的方法之一是垃圾发电技术的应用,下列说法正确的是( )
| A. | 生活垃圾焚烧处理后体积一般可减少40%~50% | |
| B. | 生活垃圾焚烧处理后体积一般可减少80%~90% | |
| C. | 因为是封闭式焚烧处理所以没有烟气排放 | |
| D. | 发出的电也有污染,不能用作生活用电 |
 .
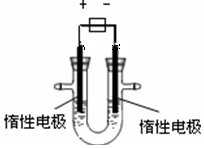
.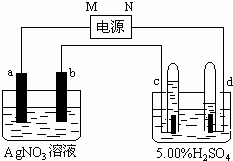 如图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极.通电一段时间后,在c、d两极上共收集到336mL(标准状态)气体.请回答下列问题.
如图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极.通电一段时间后,在c、d两极上共收集到336mL(标准状态)气体.请回答下列问题.