题目内容
4.已知工业上真空炼铷的反应方程式为:2RbCl+Mg $\stackrel{熔融}{?}$MgCl2+2Rb(g),对于此反应,能够进行正确解释的是( )| A. | 铷比镁金属性强 | |
| B. | 氯化镁比氯化铷难溶 | |
| C. | 高温下,镁离子得电子能力比铷离子弱 | |
| D. | 铷的沸点比镁低,当把铷蒸气抽走时,平衡向右反应方向移动 |
分析 2RbCl+Mg $\stackrel{熔融}{?}$MgCl2+2Rb(g)中,高温下Rb为气体,从平衡体系中逸出,生成物浓度减小,平衡正向移动,以此来解答.
解答 解:2RbCl+Mg $\stackrel{熔融}{?}$MgCl2+2Rb(g)中,铷的沸点比镁低,当把铷蒸气抽走时,平衡向右反应方向移动,则此反应可发生,与金属的金属性、盐的溶解性、离子的氧化性无关,
故选D.
点评 本题考查化学平衡的移动,为高频考点,把握浓度对平衡移动的影响为解答的关键,侧重分析与应用能力的考查,注意反应中物质的状态,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.-定条件下,合成氨反应为:N2(g)+3H2(g)?2NH3(g).图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时 间的变化曲线.图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响下列说法正确的是( )
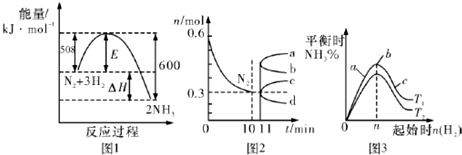

| A. | 升高温度,该反应的平衡常数增大 | |
| B. | 由图2信息,10 min内该反应的平均速率v(H2)=0.09 mol•L-1•min-1 | |
| C. | 由图2信息,从11 min起其它条件不变,压缩容器的体积,则n(N2)的变化曲线为d | |
| D. | 图3中温度T1<T2,a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是b点 |
12.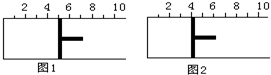 如图所示,一定条件下将lmolA气体和3molB气体充入一个体积可变的密闭容器中,可滑动活塞的位置图1所示.在恒温恒压下发生A(g)+3B(g)?2C(g),当反应达到平衡时,活塞位置如图2所示,则平衡时A的转化率为( )
如图所示,一定条件下将lmolA气体和3molB气体充入一个体积可变的密闭容器中,可滑动活塞的位置图1所示.在恒温恒压下发生A(g)+3B(g)?2C(g),当反应达到平衡时,活塞位置如图2所示,则平衡时A的转化率为( )
 如图所示,一定条件下将lmolA气体和3molB气体充入一个体积可变的密闭容器中,可滑动活塞的位置图1所示.在恒温恒压下发生A(g)+3B(g)?2C(g),当反应达到平衡时,活塞位置如图2所示,则平衡时A的转化率为( )
如图所示,一定条件下将lmolA气体和3molB气体充入一个体积可变的密闭容器中,可滑动活塞的位置图1所示.在恒温恒压下发生A(g)+3B(g)?2C(g),当反应达到平衡时,活塞位置如图2所示,则平衡时A的转化率为( )| A. | 20% | B. | 40% | C. | 50% | D. | 无法确定 |
19.可逆反应X(g)+Y(g)?2N(g)(正反应为放热反应)从反应开始到t1 s达到平衡,在t2 s末由于条件改变,平衡被破坏,在t3 s末又建立新的平衡.图中表示上述变化过程中X和N的浓度(c)与反应时间的关系.在t2 s~t3 s之间的曲线变化是由下列哪种条件改变引起的( )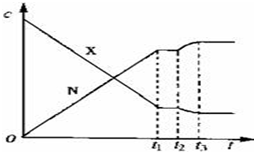

| A. | 降低温度 | B. | 增大N的浓度 | C. | 减小X的浓度 | D. | 增大压强 |
9.在容积恒定的密闭容器中,存在下列平衡:2HBr(g)?H2(g)+Br2(g)-Q,若升高温度,发生改变的是( )
| A. | 分子数 | B. | 压强 | C. | 密度 | D. | 平均摩尔质量 |
16.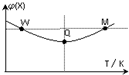 在2L恒容密闭容器中充入2mol X和1mol Y发生反应:2X(g)+Y(g)?3Z(g)△H<0,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示.下列推断正确的是( )
在2L恒容密闭容器中充入2mol X和1mol Y发生反应:2X(g)+Y(g)?3Z(g)△H<0,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示.下列推断正确的是( )
 在2L恒容密闭容器中充入2mol X和1mol Y发生反应:2X(g)+Y(g)?3Z(g)△H<0,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示.下列推断正确的是( )
在2L恒容密闭容器中充入2mol X和1mol Y发生反应:2X(g)+Y(g)?3Z(g)△H<0,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示.下列推断正确的是( )| A. | 升高温度,平衡常数增大 | |
| B. | W点X的正反应速率小于M点X的正反应速率 | |
| C. | Q点时,Y的转化率最小 | |
| D. | 平衡时充入Z,达到新平衡时Z的体积分数比原平衡时大 |
14.将下列各物质按酸、碱、盐的分类顺序排列,正确的是( )
| A. | 硫酸、纯碱、石膏 | B. | 盐酸、烧碱、小苏打 | ||
| C. | 碳酸、乙醇、硫酸钠 | D. | 磷酸、生石灰、苛性钠 |