题目内容
某结晶水合物A含有两种阳离子和一种阴离子.将溶有90.60gA的水溶液分成两等份,向第一份逐滴加入NaOH溶液,溶液先出现白色沉淀后完全溶解,此过程中产生2.24L(标准状况)刺激性气味的气体.向第二份加入过量的Ba(OH)2溶液,过滤,用稀硝酸处理沉淀物,经洗涤和干燥,得到白色固体46.60g.
请回答以下问题:
(1)试通过计算确定该结晶水合物的化学式为 ;
(2)若第二份加入75.00mL2.00mol?L-1的Ba(OH)2溶液,则得到的沉淀质量为 .
请回答以下问题:
(1)试通过计算确定该结晶水合物的化学式为
(2)若第二份加入75.00mL2.00mol?L-1的Ba(OH)2溶液,则得到的沉淀质量为
考点:化学方程式的有关计算
专题:计算题
分析:(1)能使湿润的红色石蕊试纸变蓝的气体是氨气,证明铵根离子的存在,白色溶于氢氧化钠的沉淀是氢氧化铝,和Ba(OH)2溶液反应生成的白色不溶于硝酸的白色沉淀是硫酸钡,结合电荷守恒和原子守恒来计算;
(2)过量的Ba(OH)2溶液发生NH4++Al3++2SO42-+2Ba2++5OH-=2BaSO4↓+NH3?H2O+AlO2-+2H2O,n[Ba(OH)2]=2.0mol/L×0.075L=0.15mol,若碱不足,生成沉淀为硫酸钡和氢氧化铝,结合过量判断计算.
(2)过量的Ba(OH)2溶液发生NH4++Al3++2SO42-+2Ba2++5OH-=2BaSO4↓+NH3?H2O+AlO2-+2H2O,n[Ba(OH)2]=2.0mol/L×0.075L=0.15mol,若碱不足,生成沉淀为硫酸钡和氢氧化铝,结合过量判断计算.
解答:
解:(1)一份加入足量Ba(OH)2溶液,生成白色沉淀,过滤,用稀硝酸处理沉淀物,经洗涤和干燥,得到白色固体46.6g,说明含有硫酸根离子;加入NaOH溶液,一段时间后有气体逸出,该气体有刺激性气味,能使湿润的红色石蕊试纸变蓝,该气体是氨气,证明一定含有NH4+;向其中一份逐滴加入NaOH溶液,开始发现溶液中出现白色沉淀并逐渐增多,最后白色沉淀逐渐减少并最终消失,证明一定含有Al3+,由题中信息可知45.3g的该结晶水合物中:n(SO42-)=
,n(NH4+)=
,根据离子化合物中阴、阳离子电荷平衡的原理:n(NH4+)+3n(Al3+)=2n(SO42-)可得:n(Al3+)=
(2×0.2mol-0.1 mol)=0.1 mol,n(H2O)=
=1.2mol,所以该结晶水合物中:m(NH4+):n(Al3+):n(SO42-):n(H2O)=0.1mol:0.1mol:0.2mol:1.2mol=1:1:2:12,该结晶水合物的化学式为NH4Al(SO4)2?12H2O[或(NH4)2SO4?Al2(SO4)3?24H2O],
故答案为:NH4Al(SO4)2?12H2O[或(NH4)2SO4?Al2(SO4)3?24H2O];
(2)45.3g晶体的物质的量=
,n(Ba(OH)2)=2.0mol/L×0.075L=0.15mol,n(NH4Al(SO4)2):n(Ba(OH)2)=0.1mol:0.15mol=
>
,所以氢氧化钡不足量,根据原子守恒知,生成n(BaSO4)=n(Ba(OH)2)=0.15mol,生成n(Al(OH)3)=
n(Ba(OH)2)=0.1mol,所以沉淀的质量=0.15mol×233g/mol+0.1mol×78g/mol=34.95g+7.8g=42.75g,故答案为:42.75.
| 4.66g |
| 233g/mol |
| 2.24L |
| 22.4L/mol |
| 1 |
| 3 |
| 45.3g-0.1mol×(27+18)g/mol-0.2mol×96g/mol |
| 18g/mol |
故答案为:NH4Al(SO4)2?12H2O[或(NH4)2SO4?Al2(SO4)3?24H2O];
(2)45.3g晶体的物质的量=
| 45.3g |
| 453g/mol |
| 2 |
| 3 |
| 1 |
| 2 |
| 2 |
| 3 |
点评:本题考查化学反应方程式的计算,为高频考点,把握发生的反应及离子检验、物质的量计算为解答的关键,注意守恒法及过量判断为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
相关题目
“吸烟有害于健康”.烟草燃烧释放的有害物质中,能与血红蛋白结合引起中毒的是( )
| A、尼古丁 | B、一氧化碳 |
| C、二氧化碳 | D、焦油 |
下列物质转化无法实现的是( )
A、Al2O3
| |||||
B、S
| |||||
C、Fe2O3
| |||||
D、MgCl2(aq)
|
电化学降解NO3-的原理如图所示.下列说法正确的是( )
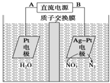

| A、电源正极为B |
| B、阳极反应式为2NO3-+6H2O+10e-=N2↑+12OH- |
| C、当产生N211.2L时,电路中通过的电子数为5NA |
| D、若电解过程中转移了2 mol电子,则两极产生的气体的质量差为10.4g |
当可逆反应2SO2(g)+O2(g)═2SO3(g)达到平衡后,向平衡体系中充入一定量的18O2气体,当反应再次达到平衡时,18O原子( )
| A、只存在于O2中 |
| B、只存于SO3中 |
| C、同时存在于O2和SO3中 |
| D、同时存在于O2、SO2和SO3中 |
下列有关物质的性质或应用正确的是( )
| A、氧化铝常用于制造耐火材料 |
| B、浓硫酸用于干燥氨气 |
| C、生产水泥的主要原料是黏土、纯碱 |
| D、Na2O用作呼吸面具的供氧剂 |
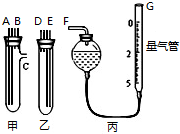 某校化学小组的同学开展测定Na2SO3和NaCl的固体混合物中Na2SO3质量分数的探究实验,他们提出下列实验方案:
某校化学小组的同学开展测定Na2SO3和NaCl的固体混合物中Na2SO3质量分数的探究实验,他们提出下列实验方案: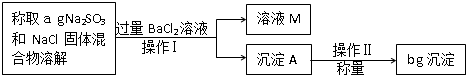
 ”标志垃圾筒的是
”标志垃圾筒的是