题目内容
20.对下列实验的评价,正确的是( )| A. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有 SO42- | |
| B. | 某无色溶液中滴入紫色石蕊试液显红色,该溶液可能有 CO 32- | |
| C. | 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有 Ba2+ | |
| D. | 验证烧碱溶液中是否含有 Cl-,先加稍过量的稀硝酸除去 OH-,再加入 AgNO3溶液,如有 白色沉淀,则证明有 Cl- |
分析 A.白色沉淀可能为AgCl或BaSO4;
B.滴入紫色石蕊试液显红色,溶液显酸性;
C.白色沉淀为碳酸钙或碳酸钡等;
D.先加稍过量的稀硝酸除去 OH-,再加入 AgNO3溶液,生成白色沉淀为AgCl.
解答 解:A.白色沉淀可能为AgCl或BaSO4,则原溶液中可能含银离子或硫酸根离子,二者不能同时存在,故A错误;
B.滴入紫色石蕊试液显红色,溶液显酸性,不能大量存在CO32-,故B错误;
C.白色沉淀为碳酸钙或碳酸钡等,则原溶液中可能含Ba2+或Ca2+,或二者均存在,故C错误;
D.先加稍过量的稀硝酸除去 OH-,再加入 AgNO3溶液,生成白色沉淀为AgCl,则证明有 Cl-,故D正确;
故选D.
点评 本题考查离子检验的实验评价,为高频考点,把握离子检验的试剂、现象与结论为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
11.科学家成功开发出便携式固体氧化物燃料电池,它以丙烷气体为燃料,空气为氧化剂,电解质是固态氧化物,在熔融状态下能传导O2-; 该电池的总反应是C3H8+5O2═3CO2+4H2O,负极反应为C3H8-20e-+10O2-═3CO2+4H2O.下列关于该燃料电池的说法中正确的是( )
| A. | 在熔融电解质中,O2-由负极移向正极 | |
| B. | 电池的正极通入丙烷 | |
| C. | 电路中每通过5 mol 电子,约有5.6 L标准状况下的丙烷被完全氧化 | |
| D. | 在电池正极的电极反应为O2-4e-═2O2- |
12.下列物质:①甲醇;②邻甲基苯酚;③甲醛;④甲酸;⑤甲酸钠;⑥甲酸甲酯,在一定条件下能与新制氢氧化铜悬浊液反应生成红色沉淀的是( )
| A. | ①②③④ | B. | ③④⑤⑥ | C. | ②③④⑤ | D. | 全部都可以 |
9.已知苯乙烯的结构为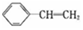 .有关该物质的下列说法正确的是( )
.有关该物质的下列说法正确的是( )
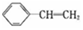 .有关该物质的下列说法正确的是( )
.有关该物质的下列说法正确的是( )| A. | 该物质在一定条件下和氢气完全加成,加成产物的一溴取代物有6种 | |
| B. | 该物质能使溴水和酸性高锰酸钾溶液褪色,褪色原理完全相同 | |
| C. | 苯乙烯分子的所有原子不可能在同一平面上 | |
| D. | 除去 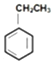 中的苯乙烯可以通入等量氢气反应 中的苯乙烯可以通入等量氢气反应 |
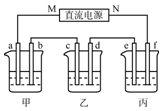 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g5%的NaOH溶液、足量的CuSO4溶液和10.00%的K2SO4溶液,电极均为石墨电极.
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g5%的NaOH溶液、足量的CuSO4溶液和10.00%的K2SO4溶液,电极均为石墨电极. 乙酸乙酯是非常重要的有机溶剂和化工原料,如图转化关系中的①、②、③是工业上合成乙酸乙酯的常见反应,其中A是一种常见的调味品.请回答:
乙酸乙酯是非常重要的有机溶剂和化工原料,如图转化关系中的①、②、③是工业上合成乙酸乙酯的常见反应,其中A是一种常见的调味品.请回答: