题目内容
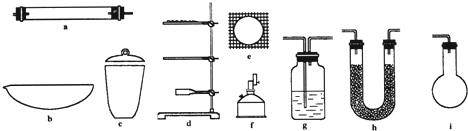
3.由短周期元素组成有关物质的转化关系如图(部分物质及条件已略),A、G是常见的金属单质,B是最常见的无色液体,C是海水中含量最高的盐类物质,电解饱和食盐水会生成氢气、氯气等,(1)K的化学式为AlCl3
(2)E的电子式为

(3)写出反应①的化学方程式2Al+2NaOH+2H2O=2NaAlO2+3H2↑

(4)写出反应②的离子方程式2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑.
分析 转化关系中各物质均由短周期元素组成,A、G是常见的金属单质,C是海水中含量最高的盐类物质,则C为NaCl,B是最常见的无色液体,B、C混合电解得到E、D、F,为电解氯化钠溶液,则B为H2O,电解得到NaOH、氢气、氯气,D与F反应得到I,金属G能与E、I反应,则G为Al,E为NaOH、I为HCl,结合转化关系可知H为NaAlO2,J为Al(OH)3,K为AlCl3,金属A与水反应得到氢氧化钠与D,则A为Na,D为H2,F为Cl2.
解答 解:转化关系中各物质均由短周期元素组成,A、G是常见的金属单质,C是海水中含量最高的盐类物质,则C为NaCl,B是最常见的无色液体,B、C混合电解得到E、D、F,为电解氯化钠溶液,则B为H2O,电解得到NaOH、氢气、氯气,D与F反应得到I,金属G能与E、I反应,则G为Al,E为NaOH、I为HCl,结合转化关系可知H为NaAlO2,J为Al(OH)3,K为AlCl3,金属A与水反应得到氢氧化钠与D,则A为Na,D为H2,F为Cl2.
(1)K的化学式为AlCl3,故答案为:AlCl3;
(2)E为NaOH,电子式为 ,故答案为:
,故答案为: ;
;
(3)反应①的化学方程式:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(4)反应②的离子方程式:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑,故答案为:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑.
点评 本题考查无机物推断,涉及Na、Al元素单质化合物性质,需要学生熟练掌握化合物知识,难度不大.

练习册系列答案
相关题目
13.下列反应的离子方程式书写正确的是( )
| A. | 氯化铝溶液与过量的氨水反应:Al3++3OH-═Al(OH)3↓ | |
| B. | 钠和硫酸铜溶液的反应:2Na+Cu2+═2Na++Cu | |
| C. | 铜与浓硝酸反应:Cu+NO3-+4H+═Cu2++NO2↑+2H2O | |
| D. | 氯气与水反应:Cl2+H2O?H++Cl-+HClO |
14.化学与工农业生产和人类生活密切相关.下列说法中,不正确的是( )
| A. | 高纯度的硅单质广泛用于制作光导纤维 | |
| B. | 油脂在碱性条件下水解可制得肥皂 | |
| C. | 海轮外壳上镶入锌块,可减缓船体的腐蚀 | |
| D. | 使用太阳能等代替化石燃料,符合低碳节能减排的要求 |
11.铁及碳的化合物在社会生产、生活中有着广泛的应用.请回答下列问题:
(1)磁铁矿是工业上冶炼铁的原料之一.
已知:①Fe3O4(s)+4C(s)?3Fe(s)+4CO(g)△H=+646.0kJ•mol-1
②C(s)+CO2(g)?2CO(g)△H=+172.5kJ•mol-1
则Fe3O4(s)+4CO(g)?3Fe(s)+4CO2(g)△H=-44.0kJ/mol.
(2)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H的平衡常数为K,在不同温度下,K值如下:
①从表中数据可推断,该反应是吸热(填“放热”或“吸热”)反应.
②温度为973K时,在某恒容密闭容器中发生上述反应.下列有关说法能说明该反应已达到平衡状态的是BD(填字母).
A.c(CO2)=c(CO) B.v正(CO2)=v逆(CO)
C.体系压强不变 D.混合气体中c(CO)不变
(3)如图图1、2表示反应:H2(g)+CO2(g)?CO(g)+H2O(g)△H>0有关量与反应时间之间的关系:
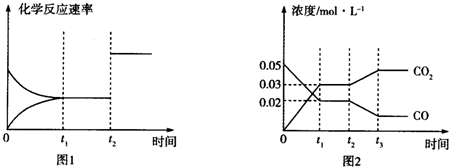
①图2中若t1=0.5min,则0~t1时间段内,H2O的平均反应速率v(H2O)=0.006mol•L-1•s-1.
②图1中t2时刻改变的条件是加入催化剂或增大压强(任写两种,下同);图2中t2时刻改变的条件是降低温度或增大水蒸气浓度或减小氢气浓度.
(4)水煤气中的CO和H2均可作为燃料电池的燃料.若在某燃料电池一极通入CO,另一极通入O2和CO2,熔融碳酸钠作为电解质,工作时负极反应式为CO+CO32--2e-=2CO2;若使用该电池电解熔融Al2O3制取10.8g Al,则理论上需要氧气的体积为6.72L
(标准状况下).
(1)磁铁矿是工业上冶炼铁的原料之一.
已知:①Fe3O4(s)+4C(s)?3Fe(s)+4CO(g)△H=+646.0kJ•mol-1
②C(s)+CO2(g)?2CO(g)△H=+172.5kJ•mol-1
则Fe3O4(s)+4CO(g)?3Fe(s)+4CO2(g)△H=-44.0kJ/mol.
(2)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H的平衡常数为K,在不同温度下,K值如下:
| 温度/K | 973 | 1173 | 1373 | 1573 |
| K | 1.47 | 2.15 | 3.36 | 8.92 |
②温度为973K时,在某恒容密闭容器中发生上述反应.下列有关说法能说明该反应已达到平衡状态的是BD(填字母).
A.c(CO2)=c(CO) B.v正(CO2)=v逆(CO)
C.体系压强不变 D.混合气体中c(CO)不变
(3)如图图1、2表示反应:H2(g)+CO2(g)?CO(g)+H2O(g)△H>0有关量与反应时间之间的关系:

①图2中若t1=0.5min,则0~t1时间段内,H2O的平均反应速率v(H2O)=0.006mol•L-1•s-1.
②图1中t2时刻改变的条件是加入催化剂或增大压强(任写两种,下同);图2中t2时刻改变的条件是降低温度或增大水蒸气浓度或减小氢气浓度.
(4)水煤气中的CO和H2均可作为燃料电池的燃料.若在某燃料电池一极通入CO,另一极通入O2和CO2,熔融碳酸钠作为电解质,工作时负极反应式为CO+CO32--2e-=2CO2;若使用该电池电解熔融Al2O3制取10.8g Al,则理论上需要氧气的体积为6.72L
(标准状况下).
18.关于有机物HC≡C-CH2CH3和CH2═CH-CH═CH2,下列说法中,不正确的是( )
| A. | 分子中所有原子都有可能处于同一平面上 | |
| B. | 都能在空气中燃烧,且燃烧时均伴有黑烟 | |
| C. | 都能被KMnO4酸性溶液氧化而使其褪色 | |
| D. | 都能与足量的溴水发生加成反应生成相同的四溴代烷 |
4.下列实验中,所采取的实验方法(或操作)与对应的原理都正确的是( )
| 选项 | 实验 | 方法(或操作) | 原理 |
| A | 分离溶于水中的溴 | 裂解汽油萃取 | 碘在裂解汽油中的溶解度较大 |
| B | 分离乙酸乙酯和乙醇 | 分液 | 乙酸乙酯和乙醇的密度不同 |
| C | 从蛋清中提取蛋白质 | 加入硫酸铜溶液 | 浓盐溶液使蛋白质溶解度降低 |
| D | 尿液中尿糖的检验 | 加入新制Cu(OH)2、加热 | 葡萄糖具有还原性 |
| A. | A | B. | B | C. | C | D. | D |
5.气态原子生成+1价气态阳离子所需要的能量称为第一电离能.元素的第一电离能是衡量元素金属性强弱的一种尺度.下列有关说法正确的是( )
| A. | 元素的第一电离能越大,其金属性越强 | |
| B. | 元素的第一电离能越小,其金属性越强 | |
| C. | 金属单质跟酸反应的难易,只跟该金属元素的第一电离能有关 | |
| D. | 同周期元素,第一电离能随原子序数增大逐渐增大 |