题目内容
将20克NaOH固体溶解于足量水中,并通入足量CO2气体,生成的溶液中各微粒浓度关系正确的是( )
| A、c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) |
| B、c(Na+)═c(HCO3-)+c(CO32-) |
| C、c(Na+)+c(H+)═c(HCO3-)+2c(CO32-)+c(OH-) |
| D、c(OH-)═c(H +)+c(HCO3-)+c(H2CO3) |
考点:离子浓度大小的比较
专题:盐类的水解专题
分析:NaOH溶液中通入足量二氧化碳,二氧化碳和NaOH溶液反应生成碳酸氢钠,碳酸氢钠溶液中HCO3-电离程度小于水解程度,导致溶液呈碱性,溶液中存在电荷守恒和物料守恒,据此分析解答.
解答:
解:NaOH溶液中通入足量二氧化碳,二氧化碳和NaOH溶液反应生成碳酸氢钠,
A.碳酸氢钠溶液中HCO3-电离程度小于水解程度,导致溶液呈碱性,HCO3-水解和水的电离都生成OH-,只有HCO3-电离生成CO32-,所以存在c(CO32-)<c(OH-),故A错误;
B.溶液中存在物料守恒,根据物料守恒得c(Na+)═c(HCO3-)+c(H2CO3)+c(CO32-),故B错误;
C.任何电解质溶液中都存在电荷守恒,根据电荷守恒得c(Na+)+c(H+)═c(HCO3-)+2c(CO32-)+c(OH-),故C正确;
D.根据物料守恒得c(Na+)═c(HCO3-)+c(H2CO3)+c(CO32-),根据电荷守恒得c(Na+)+c(H+)═c(HCO3-)+2c(CO32-)+c(OH-),所以得c(H2CO3)+c(H+)═c(CO32-)+c(OH-),故D错误;
故选C.
A.碳酸氢钠溶液中HCO3-电离程度小于水解程度,导致溶液呈碱性,HCO3-水解和水的电离都生成OH-,只有HCO3-电离生成CO32-,所以存在c(CO32-)<c(OH-),故A错误;
B.溶液中存在物料守恒,根据物料守恒得c(Na+)═c(HCO3-)+c(H2CO3)+c(CO32-),故B错误;
C.任何电解质溶液中都存在电荷守恒,根据电荷守恒得c(Na+)+c(H+)═c(HCO3-)+2c(CO32-)+c(OH-),故C正确;
D.根据物料守恒得c(Na+)═c(HCO3-)+c(H2CO3)+c(CO32-),根据电荷守恒得c(Na+)+c(H+)═c(HCO3-)+2c(CO32-)+c(OH-),所以得c(H2CO3)+c(H+)═c(CO32-)+c(OH-),故D错误;
故选C.
点评:本题考查离子浓度大小比较,明确溶液中溶质及其性质是解本题关键,灵活运用守恒思想解答问题,易错选项是A,会比较氢氧根离子和碳酸根离子浓度相对大小,为易错点.

练习册系列答案
相关题目
关于电解氯化钠溶液,下列叙述正确的是( )
| A、电解时在阳极得到氯气,在阴极得到金属钠 |
| B、在阳极附近有黄绿色的气体产生 |
| C、在阴极附近的溶液中滴入酚酞溶液,溶液呈无色 |
| D、电解一段时间后,将电解液全部转移到烧杯中,充分搅拌后溶液呈中性 |
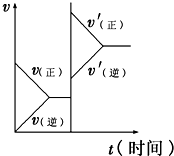 对于达到平衡的可逆反应:X+Y?W+Z,增大压强则正、逆反应速率(v)的变化如图所示,分析可知X、Y、Z、W的聚集状态可能是( )
对于达到平衡的可逆反应:X+Y?W+Z,增大压强则正、逆反应速率(v)的变化如图所示,分析可知X、Y、Z、W的聚集状态可能是( )| A、X、Y、Z、W均为气体 |
| B、Z、W为气体,X、Y中之一为气体 |
| C、X、Y、Z皆为气体,W为非气体 |
| D、X、Y为气体,Z、W中至少有一种为气体 |
在120℃时,某混合烃和过量O2在一密闭容器中完全反应,测知反应前后的压强没有变化,则该混合烃不可能是( )
| A、CH4和C2H4 |
| B、C2H2和C2H6 |
| C、C2H4和C3H4 |
| D、C4H8和C3H6 |
如图所示仪器可用于实验室制备少量无水FeCl3,仪器连接顺序正确的是( ) 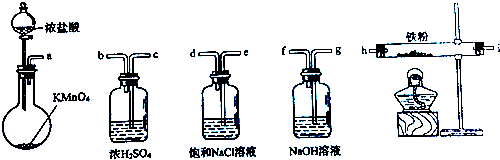

| A、a-b-c-d-e-e-f-g-h |
| B、a-e-d-c-b-h-i-g |
| C、a-d-e-c-b-h-i-g |
| D、a-c-b-d-e-h-i-f |
下列说法正确的是( )
| A、相对分子质量相近的醇比烷烃沸点高是因为醇分子间存在氢键 |
| B、苯和油脂均不能使酸性高锰酸钾溶液褪色 |
| C、红外光谱分析不能区分乙醇和乙酸乙酯 |
| D、蛋白质溶液中加硫酸铵或氯化铜溶液,均会发生蛋白质的变性 |

 在密闭容器中加入等浓度的CO与H2O,T℃时发生如下反应:
在密闭容器中加入等浓度的CO与H2O,T℃时发生如下反应: